题目内容
【题目】室温下,向一定体积的![]() 的
的![]() 溶液中逐滴加入
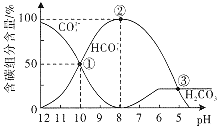
溶液中逐滴加入![]() 盐酸至过量,溶液中含碳元素的各微粒的物质的量浓度的百分含量随溶液pH的变化如图所示
盐酸至过量,溶液中含碳元素的各微粒的物质的量浓度的百分含量随溶液pH的变化如图所示![]() 因逸出未画出,滴加盐酸的过程中温度的变化忽略不计
因逸出未画出,滴加盐酸的过程中温度的变化忽略不计![]() 。下列说法正确的是
。下列说法正确的是![]()
A.点![]() 时溶液中水的电离程度比纯水的大
时溶液中水的电离程度比纯水的大
B.点![]() 所示溶液中:
所示溶液中:![]()
C.当滴加盐酸到点![]() 时,才开始放出
时,才开始放出![]() 气体
气体
D.![]() 第一步水解反应的平衡常数:
第一步水解反应的平衡常数:![]()
【答案】A
【解析】
![]() 点
点![]() 溶液中为等浓度的碳酸钠和碳酸氢钠混合溶液,溶液显碱性,碳酸根离子水解为主,盐类水解促进水的电离,点
溶液中为等浓度的碳酸钠和碳酸氢钠混合溶液,溶液显碱性,碳酸根离子水解为主,盐类水解促进水的电离,点![]() 时溶液中水的电离程度比纯水的大,选项A正确;
时溶液中水的电离程度比纯水的大,选项A正确;
B.点![]() 所示溶液中含C元素的微粒有
所示溶液中含C元素的微粒有![]() 、
、![]() ,且滴加盐酸后溶液体积增大,物料守恒可知,
,且滴加盐酸后溶液体积增大,物料守恒可知,![]() ,选项B错误;
,选项B错误;
C.图象可知![]() 时,
时,![]() 的量保持不变,说明
的量保持不变,说明![]() 时,二氧化碳在溶液中已达到饱和,之后就会有二氧化碳气体放出,选项C错误;
时,二氧化碳在溶液中已达到饱和,之后就会有二氧化碳气体放出,选项C错误;
D.平衡常数只随温度变化,温度不变平衡常数不变,![]() 第一步水解反应的平衡常数:
第一步水解反应的平衡常数:![]() ,选项D错误;
,选项D错误;
答案选A。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
【题目】硫酸亚铁铵![]() 又称莫尔盐,是浅绿色晶体。用硫铁矿
又称莫尔盐,是浅绿色晶体。用硫铁矿![]() 主要含
主要含![]() 、
、![]() 等
等![]() 制备莫尔盐的流程如下:
制备莫尔盐的流程如下:
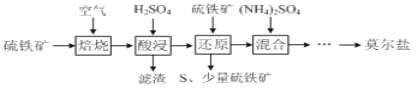
已知:“还原”时,![]() 与
与![]() 不反应,
不反应,![]() 通过反应Ⅰ、Ⅱ被还原,反应Ⅰ如下:
通过反应Ⅰ、Ⅱ被还原,反应Ⅰ如下:![]()
![]() 写出“还原”时
写出“还原”时![]() 与
与![]() 发生还原反应Ⅱ的离子方程式:__________。
发生还原反应Ⅱ的离子方程式:__________。
实验室检验“还原”已完全的方法是__________。
![]() “还原”前后溶液中部分离子的浓度见下表
“还原”前后溶液中部分离子的浓度见下表![]() 溶液体积变化忽略不计
溶液体积变化忽略不计![]() ,请计算反应Ⅰ、Ⅱ中被还原的Fe
,请计算反应Ⅰ、Ⅱ中被还原的Fe![]() 的物质的量之比__________。
的物质的量之比__________。
离子 | 离子浓度 | |
还原前 | 还原后 | |
|
|
|
|
|
|
![]() 称取
称取![]() 新制莫尔盐,溶于水配成250mL溶液。取
新制莫尔盐,溶于水配成250mL溶液。取![]() 该溶液加入足量的
该溶液加入足量的![]() 溶液,得到白色沉淀
溶液,得到白色沉淀![]() ;另取
;另取![]() 该溶液用
该溶液用![]() 酸性溶液滴定,当
酸性溶液滴定,当![]() 恰好完全被还原为
恰好完全被还原为![]() 时,消耗溶液的体积为
时,消耗溶液的体积为![]() 。试确定莫尔盐的化学式
。试确定莫尔盐的化学式![]() 请写出计算过程)________________。
请写出计算过程)________________。