题目内容
(2009?湛江二模)从下列事实所得出的相应结论正确的是( )
|
分析:①根据电解质的定义分析;
②根据强酸准备弱酸的特点判断;
③Na[Al(OH)4]促进HCO3-的电离;
④比较非金属性的角度错误;
⑤能使湿润红色石蕊试纸变蓝的气体为氨气.
②根据强酸准备弱酸的特点判断;
③Na[Al(OH)4]促进HCO3-的电离;
④比较非金属性的角度错误;
⑤能使湿润红色石蕊试纸变蓝的气体为氨气.
解答:解:①电解质应是化合物,氯气既不是电解质也不是非电解质,故①错误;
②二氧化碳溶于水生成碳酸,通入Na2SiO3溶液中产生白色浑浊,说明生成硅酸,则酸性:H2CO3>H2SiO3,符合强酸准备弱酸的特点,故②正确;
③Na[Al(OH)4]促进HCO3-的电离,产生白色沉淀,可说明酸性:HCO3->Al(OH)3,故③正确;
④氮气中存在N≡N,键能较大,导致氮气在常温下较稳定,非金属性N>P,可通过对应的最高价氧化物的水化物比较,故④错误;
⑤能使湿润红色石蕊试纸变蓝的气体为氨气,可说明有NH4+,故⑤正确.
故选B.
②二氧化碳溶于水生成碳酸,通入Na2SiO3溶液中产生白色浑浊,说明生成硅酸,则酸性:H2CO3>H2SiO3,符合强酸准备弱酸的特点,故②正确;
③Na[Al(OH)4]促进HCO3-的电离,产生白色沉淀,可说明酸性:HCO3->Al(OH)3,故③正确;
④氮气中存在N≡N,键能较大,导致氮气在常温下较稳定,非金属性N>P,可通过对应的最高价氧化物的水化物比较,故④错误;
⑤能使湿润红色石蕊试纸变蓝的气体为氨气,可说明有NH4+,故⑤正确.
故选B.
点评:本题考查化学实验方案的评价,涉及物质的检验、鉴别、制备以及电解质与非电解质的比较等,综合考查学生化学知识的应用和实验评价能力,注意把握物质的性质以及实验方案的设计,题目难度中等.

练习册系列答案
相关题目
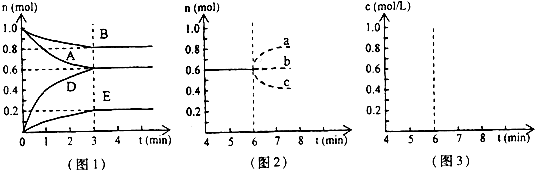
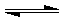 pD(g)+qE(s),△H<0(m、n、p、q为最简整数比).
pD(g)+qE(s),△H<0(m、n、p、q为最简整数比).