��Ŀ����
����Ŀ��ij���Թ�ҵ��ˮ�к���K2Cr2O7 �� �����£����ᣨH2C2O4���ܽ����е�Cr2O72��ת��ΪCr3+ �� ij�������о����֣�����������[Al2Fe��SO4��424H2O]���ɶԸ÷�Ӧ������ã�Ϊ��һ���о��й����ضԸ÷�Ӧ���ʵ�Ӱ�죬̽�����£�
��1����25���£����ƹ���ǿ�ȡ���ˮ��Ʒ��ʼŨ�Ⱥʹ���������ͬ�����ڲ�ͬ�ij�ʼpH��һ��Ũ�Ȳ�����Һ���������Ա�ʵ�飬�������ʵ����Ʊ�
ʵ���� | ��ʼpH | ��ˮ��Ʒ���/mL | ������Һ���/mL | ����ˮ���/mL |
�� | 4 | 60 | 10 | 30 |
�� | 5 | 60 | 10 | 30 |
�� | 5 | 60 |
���ʵ��ٺ͢���Һ�е�Cr2O72��Ũ����ʱ��仯��ϵ��ͼ��ʾ��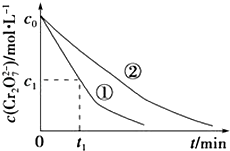
��2��������Ӧ����ᱻ���������ӷ���ʽΪ
��3��ʵ��ٺ͢ڵĽ��������ʵ�����0��t1ʱ��η�Ӧ����v��Cr3+��=molL��1min��1���ô���ʽ��ʾ����
��4���ÿ������������[Al2Fe��SO4��424H2O]��������õijɷ�������¼��裬������ɼ�����ͼ������� ����һ��Fe2+������ã�
���������
����������
��5���������ʵ����֤��������һ������±������ݣ� ����������ʵ���ṩ���Լ��⣬�ɹ�ѡ���ҩƷ��K2SO4��FeSO4��K2SO4Al2��SO4��324H2O��Al2��SO4��3�ȣ���Һ��Cr2O72����Ũ�ȿ��������ⶨ��
ʵ�鷽������Ҫ��д����������̣� | Ԥ��ʵ�����ͽ��� |
���𰸡�
��1��20��20
��2��Cr2O72��+3H2C2O4+8H+=6CO2��+2Cr3++7H2O
��3����ҺPH�Ը÷�Ӧ��������Ӱ�죻 ![]()
��4��Al3+������ã� SO42���������
��5���õ����ʵ���K2SO4?Al2��SO4��3?24H2O����ʵ����е�������,����������Ӧ������ʵ�����ͬ,���жԱ�ʵ�飻��Ӧ������ͬʱ���,����Һ��c��Cr2O72��������ʵ�����c��Cr2O72����,�����һ������������Һ�е�c��Cr2O72������ͬ,�����һ������
���������⣺��1���٢���PH��ͬ����̽��PH�����ʵ�Ӱ�죻��ڢ���̽����ͬŨ��ʱ��������ʵ�Ӱ�죬���Դ��ǣ�
ʵ���� | ��ʼ pH | ��ˮ��Ʒ ���/mL | ������Һ ���/mL | ����ˮ ���/mL |
�� | 20 | 20 |
����2��������̼Ԫ�ػ��ϼ�Ϊ+3�ۣ���������ΪCO2��������Ϊ+4�ۣ����ϼ۹�����2�ۣ�Cr2O72��ת��ΪCr3+�����ϼ۹�������6�ۣ����ݵ����غ㣬�μӷ�Ӧ��Cr2O72�����������ʵ���֮��Ϊ��1��3�����ӷ���ʽΪ��Cr2O72��+3H2C2O4+8H+=6CO2��+2Cr3++7H2O��
���Դ��ǣ�Cr2O72��+3H2C2O4+8H+=6CO2��+2Cr3++7H2O����3����ʵ��٢ڱ�����ҺpHԽС����Ӧ������Խ�죬������ҺpH�Ը÷�Ӧ��������Ӱ�죬v��Cr3+��=2v��Cr2O72����= ![]() molL��1min��1��
molL��1min��1��
���Դ��ǣ���ҺpH�Ը÷�Ӧ��������Ӱ�죻 ![]() ����4������������[Al2Fe��SO4��424H2O]��ɷ�����Al3+������ã�SO42��������ã�
����4������������[Al2Fe��SO4��424H2O]��ɷ�����Al3+������ã�SO42��������ã�
���Դ��ǣ�Al3+������ã�SO42��������ã���5��Ҫ֤��Fe2+������ã������Ա�ʵ�飬����û��Fe2+����ʱ��ʵ�飬����ҪѡK2SO4Al2��SO4��324H2O��ע��������Ҫ����Al3+��SO42��Ũ�ȱȣ���Ҫѡ��K2SO4��Al2��SO4��3���õ����ʵ���K2SO4Al2��SO4��324H2O����ʵ����е�������������������Ӧ������ʵ�����ͬ�����жԱ�ʵ�飬��Ӧ������ͬʱ�������Һ��c��Cr2O72��������ʵ�����c��Cr2O72�����������һ������������Һ�е�c��Cr2O72������ͬ�������һ�����������Դ��ǣ�
ʵ�鷽�� | Ԥ��ʵ�����ͽ��� |
�õ����ʵ���K2SO4Al2��SO4��324H2O����ʵ����е�������������������Ӧ������ʵ�����ͬ�����жԱ�ʵ�� | ��Ӧ������ͬʱ�������Һ��c��Cr2O72��������ʵ�����c��Cr2O72�����������һ������������Һ�е�c��Cr2O72������ͬ�������һ������ |