题目内容
【题目】(i)燃料电池是目前正在探索的一种新型电池,目前已经使用的氢氧燃料电池的基本反应是正极:O2+2H2O+4e-=4OH-,回答下列问题:
(1)电解质溶液为____________。
(2)负极发生________反应(填“氧化”或“还原”)。写出其电极反应式___________。
(3)若反应后得到5.4 g液态水,此时氢氧燃料电池转移的电子数为________。
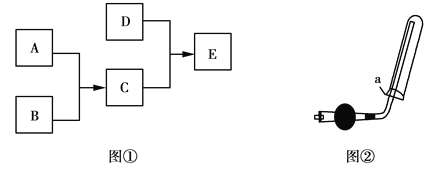
(ii)如图所示的装置,在盛有水的烧杯中,铁圈和银圈的连接处吊着一根绝缘的细丝,使之平衡。小心地往烧杯中央滴入CuSO4溶液。

(1)片刻后可观察到的现象是(指悬吊的金属圈)________。
A.铁圈和银圈左右摇摆不定 B.保持平衡状态不变
C.铁圈向下倾斜 D.银圈向下倾斜
(2)产生上述现象的原因是___________________________________。
(iii)铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式:___________________________。
(2)若将(1)中的反应设计成原电池,并写出正、负极电极反应式。
正极反应:______________________,负极反应:______________________。
【答案】 KOH 氧化 H2+2OH--2e-===2H2O 0.6NA D 加入CuSO4溶液后,构成Fe-Ag原电池,铁溶解,质量减轻,Cu2+在银圈上得电子,生成Cu沉积在其上,质量增加 2Fe3++Cu===2Fe2++Cu2+ 2Fe3++2e-===2Fe2+ Cu-2e-===Cu2+
【解析】分析:(i)根据正极产生氢氧根判断电解质溶液的酸碱性;根据原电池的工作原理解答;根据总反应式计算转移电子数;
(ii)小心地往烧杯中央滴入CuSO4溶液后构成原电池,结合原电池的工作原理解答。
(iii)(1)FeCl3溶液与铜反应生成氯化亚铁和氯化铜;
(2)根据原电池的工作原理结合铁离子和铜的性质解答。
详解:(1)氢氧燃料电池的正极反应式为O2+2H2O+4e-=4OH-,正极产生氢氧根,这说明电解质溶液为碱性溶液,例如KOH。
(2)原电池的负极发生失去电子的氧化反应,则负极发生氧化反应,因此氢气在负极通入,则其电极反应式为H2+2OH--2e-=2H2O;
(3)总反应式为O2+2H2=2H2O,即生成36g水转移4mol电子,因此若反应后得到5.4 g液态水,则此时氢氧燃料电池转移的电子数为![]() =0.6NA。
=0.6NA。
(ii)(1)小心地往烧杯中央滴入CuSO4溶液后构成原电池,金属性铁大于银,因此铁是负极,失去电子转化为亚铁离子,质量减小。溶液中的铜离子在正极银电极表面放电析出铜,质量增加,所以片刻后可观察到的现象是银圈向下倾斜,答案选D;
(2)根据以上分析可知产生上述现象的原因是加入CuSO4溶液后,构成Fe-Ag原电池,铁溶解,质量减轻,Cu2+在银圈上得电子,生成Cu沉积在其上,质量增加。
(iii)(1)FeCl3溶液与铜反应生成氯化亚铁和氯化铜,反应的方程式为2Fe3++Cu=2Fe2++Cu2+;
(2)根据方程式可知铜失去电子,则铜是负极,电极反应式为Cu-2e-=Cu2+。溶液中的铁离子得到电子,在正极放电,则正极反应为2Fe3++2e-=2Fe2+。