题目内容
(15分)
原子序数依次递增的X、Y、Z、W是周期表中前30号元素,其中只有X、Y同周期。已知X的最外层电子数是其内层电子数的2倍;X与Y形成的常见化合物之一常被用于高炉炼铁;Z与X同主族,其单质在同周期元素形成的单质中熔点最高;W原子M能层为全充满状态,且核外的未成对电子只有一个。回答下列问题:
(1)从电负性角度分析,X,Y,Z三种元素的非金属活泼性由强到弱的顺序为 。
(2)X、Y分别与H形成的化学键的极性关系为X-H Y-H(填“<”、“>”或“=”)。
(3)+l价气态基态阳离子再失去一个电子形成+2价气态基态阳离子所需要的能量称为第二电离能I2,依次还有I3、I4、I5…,推测Z元素的电离能突增应出现在第____电离能。
(4)X的氢化物中X原子的杂化方式为sp2,则相对分子质量最小的分子式为____,
(5)W的价电子排布图为 ;下图____表示的是W晶体中微粒的堆积方式(填甲、乙或丙);若W晶体中一个晶胞的边长为a cm,则W晶体的密度为____(写出含a的表达式,用NA表示阿伏伽德罗常数)。

(15分) (1)O>C >Si (2分)
(2)< (2分)
(3)第五 (2分)
(4)C2H4,(2分)
 (5)
(2分) 丙(2分)
(5)
(2分) 丙(2分) 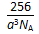 g/cm3(3分)
g/cm3(3分)
【解析】本题综合考察了物质结构与性质相关知识。(1)通过题干信息,推出X、Y、Z、W分别是C、O、Si、Cu元素,不难推出X,Y,Z三种元素的非金属活泼性强弱。(2)由于O元素的电负性大于C元素,所有C-H < O-H(3)Si的最外层电子数为4,所有第五个电子失去会出现电离能突增应。(4)C原子的sp2杂化方式,应该还剩下一个p电子成双键,所以最小分子式为C2H4, (5)Cu的价电子排布3d104s1,其晶体中微粒的堆积方式为面心立方最密堆积,所以堆积方式选择丙。用均摊法推知面心立方最密堆积Cu晶体中一个晶胞含有4个Cu原子,进行相关计算。

 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案| A、D元素处于元素周期表中第3周期第IV族 | B、四种元素的原子半径:A<B<D<C | C、B、D的最高价氧化物中,B、D与氧原子之间均为双键 | D、一定条件下,B单质能置换出D单质,C单质能置换出A单质 |
 [化学选修3:物质结构与性质]
[化学选修3:物质结构与性质]