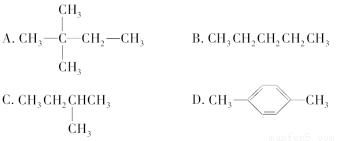题目内容
(12分)溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物。某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究。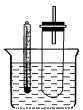
实验操作Ⅰ:在试管中加入5 mL 1 mol/L NaOH溶液和5 mL溴乙烷,振荡。
实验操作Ⅱ:将试管如图固定后,水浴加热。
(1)用水浴加热而不直接用酒精灯加热的原因是 ;试管口安装一长导管的作用是 。
(2)鉴定生成物中乙醇的结构,可用的波谱是 , 。
(3)为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,在你设计的实验方案中,需要检验的是 ,检验的方法是 (需说明所用的试剂、简单的实验操作及预测产生的实验现象)。
(1)使试管受热均匀 冷凝回流,减少溴乙烷的损失
(2)红外光谱、核磁共振氢谱
(3)生成的气体 将生成的气体先通过盛有水的试管,再通入盛有酸性KMnO4溶液的试管,观察酸性KMnO4溶液是否褪色(或直接通入溴的四氯化碳溶液)
【解析】
试题分析:(1)因为溴乙烷沸点低,所以采用水浴加热,因此水浴加热的目的是使试管受热均匀,且温度不会太高;试管口安装一长导管的作用是冷凝回流,减少溴乙烷的损失
(2)红外光谱可以鉴定物质中官能团的存在,核磁共振氢谱用来测定氢原子的种数,所以可采用红外光谱、核磁共振氢谱来鉴定其结构
(3)溴乙烷在NaOH乙醇溶液中发生的是消去反应,产物是乙烯,所以需验证生成的气体成分,其操作步骤为将产生的气体通入溴的四氯化碳溶液中,观察溴的四氯化碳溶液是否褪色;或将生成的气体先通过盛有水的试管,再通入盛有酸性KMnO4溶液的试管,观察酸性KMnO4溶液是否褪色
考点:考查溴乙烷的水解和消去反应的条件及对实验装置的判断,鉴定物质结构用到的方法

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案某温度下,密闭容器中X、Y、Z、W四种气体的初始浓度和平衡浓度如下表,下列说法错误的是
物质 | X | Y | Z | W |
初始浓度/mol·L-1 | 0.5 | 0.6 | 0 | 0 |
平衡浓度/mol·L-1 | 0.1 | 0.1 | 0.4 | 0.6 |
A.反应达到平衡时,X的转化率为80%
B.该反应的平衡常数表达式为K=
C.增大压强其平衡常数不变,但使平衡向生成Z的方向移动
D.改变温度可以改变此反应的平衡常数