题目内容
【题目】A、B、C、D、E五种化合物,均含有某种常见元素,它们的转化关系如下图所示,其中A为澄清溶液,C为难溶于水的白色固体,E则易溶于水,若取A溶液灼烧,焰色反应为浅紫色(透过蓝色钴玻璃)。
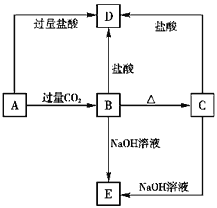
请回答下列问题:
(1)写出化学式:A________。
(2)写出下列反应的离子方程式:
A→B___________________________________。
B→D_________________________________。
C→E_________________________________。
【答案】 KAlO2 ![]() +CO2+2H2O===Al(OH)3↓+
+CO2+2H2O===Al(OH)3↓+![]() Al(OH)3+3H+===Al3++3H2O Al2O3+2OH===2
Al(OH)3+3H+===Al3++3H2O Al2O3+2OH===2![]() +H2O
+H2O
【解析】(1)分析题中的转化关系发现,B、C两种物质都既能与强酸反应,又都能与强碱反应,所以是两性化合物,因此可从铝元素入手思考,进而确定B是Al(OH)3,C是Al2O3,则D是AlCl3,E是偏铝酸钠, 由A![]() B,且A溶液的焰色反应呈浅紫色,所以A为KAlO2。
B,且A溶液的焰色反应呈浅紫色,所以A为KAlO2。
(2) 根据(1)的分析写出反应的离子方程式为:
A→B反应的离子方程式为:AlO2-+CO2+2H2O![]() Al(OH)3↓+HCO3-
Al(OH)3↓+HCO3-
B→D反应的离子方程式为:Al(OH)3+3H+=Al3++3H2O
C→E反应的离子方程式为:Al2O3+2OH-=2AlO2-+H2O

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目