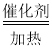题目内容
【题目】一定条件下,在水溶液中1molCl-、ClOx-(x=1、2、3、4)的能量(kJ)相对大小如图所示。下列说法正确的是( )
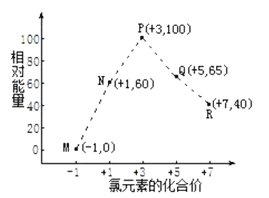
A.P点对应的微粒最稳定
B.R点微粒氧化性最强
C.由N点到M点的焓变为60kJ·mol-1
D.P点微粒发生歧化反应转化为N点和Q点微粒属于自发过程
【答案】D
【解析】
A.依据图示M、N、P、Q、R点中M点Cl-能量最低,所以最稳定,故A错误;
B.M、N、P、Q、R中,P点为次氯酸根离子,氧化性最强,故B错误;
C.由N点到M点能量降低,焓变值为负,故C错误;
D.依据图示可知:2ClO2-=ClO3-+ClO-,反应热=(60kJ/mol+65kJ/mol)-2×100kJ/mol=-80kJ/mol,热化学方程式为,2ClO2-(aq)=ClO3-(aq)+ClO-(aq)△H=-80 kJmol-1,依据热化学方程式可知:△H<0,△S变化不大,所以△H-T△S<0,反应能自发进行,故D正确;
故选:D。

练习册系列答案
相关题目
【题目】利用下图装置可以进行实验并能达到实验目的的是
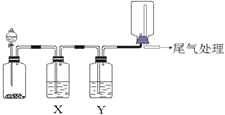
选项 | 实验目的 | X中试剂 | Y中试剂 |
A[] | 用MnO2和浓盐酸制取并收集纯净干燥的Cl2 | 饱和食盐水 | 浓硫酸 |
B | 用Cu与稀硝酸制取并收集纯净干燥的NO | 水 | 浓硫酸 |
C | 验证电石与饱和食盐水反应生成的气体的性质并收集 | CuSO4溶液 | KMnO4 |
D | CaCO3和稀盐酸制取并收集纯净干燥的CO2 | 饱和NaHCO3溶液 | 浓硫酸 |
A. A B. B C. C D. D