题目内容
 电解原理在化学工业中有广泛应用.如图所示,在U形管中加入NaCl溶液,在两极各滴入几滴石蕊试液,插入惰性电极,接通电源.
电解原理在化学工业中有广泛应用.如图所示,在U形管中加入NaCl溶液,在两极各滴入几滴石蕊试液,插入惰性电极,接通电源.(1)①一段时间后可观察到的Y电极附近观察到的现象是
溶液呈蓝色并有气泡产生
溶液呈蓝色并有气泡产生
.②X电极上的电极反应式为
2Cl--2e-=Cl2↑,
2Cl--2e-=Cl2↑,
,③请写出电解饱和NaCl溶液的化学方程式2NaCl+2H2O
2NaOH+Cl2↑+H2↑
| ||
2NaCl+2H2O
2NaOH+Cl2↑+H2↑
.
| ||
(2)如果电解液a选用CuCl2溶液,则在电解过程中被氧化的是:
Cl-
Cl-
在此变化过程中发生的能量转化的形式是电能转化为化学能
电能转化为化学能
.分析:(1)①根据电极判断生成物,从而确定反应现象;
②根据离子放电顺序判断生成物并写出电极反应式;
③阴阳极上电极反应式相加得电池反应式;
(2)根据得失电子判断被氧化的离子,根据电解池的定义分析.
②根据离子放电顺序判断生成物并写出电极反应式;
③阴阳极上电极反应式相加得电池反应式;
(2)根据得失电子判断被氧化的离子,根据电解池的定义分析.
解答:解:(1)①根据图知,Y电极为阴极,氢离子在阴极上得电子生成氢气,所以Y电极附近氢离子浓度降低,氢氧根离子浓度增大,溶液呈碱性,加入石蕊试液溶液呈蓝色,故观察到的现象是:溶液呈蓝色并有气泡产生.
故答案为:溶液呈蓝色并有气泡产生;
②氯离子的放电能力大于氢氧根离子,所以X电极上氯离子失电子生成氯气,电极反应式为2Cl--2e-=Cl2↑.
故答案为:2Cl--2e-=Cl2↑;
③通过以上分析知,氯化钠和水在电解条件下生成氢气、氯气和氢氧化钠,所以电池反应式为
2NaCl+2H2O
2NaOH+Cl2↑+H2↑,
故答案为:2NaCl+2H2O
2NaOH+Cl2↑+H2↑;
(2)如果电解液a选用CuCl2溶液,失电子的离子为Cl-,所以Cl-被氧化;该装置借助外加电源,所以是将电能转化为化学能.
故答案为:Cl-;电能转化为化学能.
故答案为:溶液呈蓝色并有气泡产生;
②氯离子的放电能力大于氢氧根离子,所以X电极上氯离子失电子生成氯气,电极反应式为2Cl--2e-=Cl2↑.
故答案为:2Cl--2e-=Cl2↑;
③通过以上分析知,氯化钠和水在电解条件下生成氢气、氯气和氢氧化钠,所以电池反应式为
2NaCl+2H2O
| ||
故答案为:2NaCl+2H2O
| ||
(2)如果电解液a选用CuCl2溶液,失电子的离子为Cl-,所以Cl-被氧化;该装置借助外加电源,所以是将电能转化为化学能.
故答案为:Cl-;电能转化为化学能.
点评:本题考查了电解池中电极反应式的书写及电解池的反应现象等知识点,只有明确溶液中离子的放电顺序,才能正确书写电极反应式.

练习册系列答案
相关题目
 (1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是
 电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.请回答以下问题: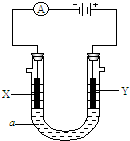 (I)Li-SOCl2电池可用于心脏起搏器.该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2.电池的总反应可表示为:4Li+2SOCl2=4LiCl+S+SO2.
(I)Li-SOCl2电池可用于心脏起搏器.该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2.电池的总反应可表示为:4Li+2SOCl2=4LiCl+S+SO2. 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X,Y是两块电极板,通过导线与直流电源相连.
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X,Y是两块电极板,通过导线与直流电源相连.