题目内容
(7分)短周期元素Q、R、T、W在元素周期表中的位置如右图所示,其中T所处的周期序数与主族序数相等,请回答下列问题:

(1)T的原子结构示意图为 ;
(2)Q的最高价氧化物水化物的酸性 W的最高价氧化物水化物的酸性,则元素的非金属性:Q W(填“>”或“<”);
(3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,一种是液体,另一种是气体,该气体能使品红溶液褪色,则反应的化学方程式为 ;
(4)R有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L的甲气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是 ;

(1)T的原子结构示意图为 ;
(2)Q的最高价氧化物水化物的酸性 W的最高价氧化物水化物的酸性,则元素的非金属性:Q W(填“>”或“<”);
(3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,一种是液体,另一种是气体,该气体能使品红溶液褪色,则反应的化学方程式为 ;
(4)R有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L的甲气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是 ;
(1) (1分) (2)< (1分) < (1分)
(1分) (2)< (1分) < (1分)
(3)S+2H2SO4(浓) 3SO2↑+2H2O (2分)
3SO2↑+2H2O (2分)
(4)NaNO2;(2分)
 (1分) (2)< (1分) < (1分)
(1分) (2)< (1分) < (1分)(3)S+2H2SO4(浓)
 3SO2↑+2H2O (2分)
3SO2↑+2H2O (2分)(4)NaNO2;(2分)
“T所处的周期序数与主族序数相等”,同时结合图的结构可知:T处于第三周期IIIA族,所以,T为铝元素;则Q为碳元素、R为氮元素,W为硫元素;
(2)碳酸是弱酸,硫酸是强酸,故Q的最高价氧化物水化物的酸性<W的最高价氧化物水化物的酸性;而最高价氧化物对应水化物的酸性越强,则原子的得电子能力越强,元素的非金属性越强;
(3)“该气体能使品红溶液褪色”,所以该气体为SO2,再利用原子守恒得:另一液体产物为水;根据题目的叙述即可得出反应的方程式:S+2H2SO4(浓) 3SO2↑+2H2O(S与浓H2SO4发生了氧化还原反应,故应利用化合价升降相等配平方程式)
3SO2↑+2H2O(S与浓H2SO4发生了氧化还原反应,故应利用化合价升降相等配平方程式)
(4)R的+1、+2、+3、+4、+5价都有氧化物,其中NO的相对分子质量最小,则甲为NO;
“2L的甲气体与0.5L的氧气相混合”
2NO + O2 = 2NO2,
2 1 2
1L 0.5L 1L
则反应后变为1LNO与1LNO2(即在同温同压下,两者等物质的量)的混合物,再“该混合气体被足量的NaOH溶液完全吸收后没有气体残留”说明反应为:NO+NO2+2NaOH=2NaNO2+H2O(发生了氧化还原反应,NO中N为+2价,NO2中N为+4价,故两者发生归中反应,生成+3价,故为NaNO2)
(2)碳酸是弱酸,硫酸是强酸,故Q的最高价氧化物水化物的酸性<W的最高价氧化物水化物的酸性;而最高价氧化物对应水化物的酸性越强,则原子的得电子能力越强,元素的非金属性越强;
(3)“该气体能使品红溶液褪色”,所以该气体为SO2,再利用原子守恒得:另一液体产物为水;根据题目的叙述即可得出反应的方程式:S+2H2SO4(浓)
 3SO2↑+2H2O(S与浓H2SO4发生了氧化还原反应,故应利用化合价升降相等配平方程式)
3SO2↑+2H2O(S与浓H2SO4发生了氧化还原反应,故应利用化合价升降相等配平方程式)(4)R的+1、+2、+3、+4、+5价都有氧化物,其中NO的相对分子质量最小,则甲为NO;
“2L的甲气体与0.5L的氧气相混合”
2NO + O2 = 2NO2,
2 1 2
1L 0.5L 1L
则反应后变为1LNO与1LNO2(即在同温同压下,两者等物质的量)的混合物,再“该混合气体被足量的NaOH溶液完全吸收后没有气体残留”说明反应为:NO+NO2+2NaOH=2NaNO2+H2O(发生了氧化还原反应,NO中N为+2价,NO2中N为+4价,故两者发生归中反应,生成+3价,故为NaNO2)

练习册系列答案
相关题目
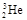 是较为安全的高效核聚变反应原料。
是较为安全的高效核聚变反应原料。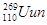 。该原子的原子核内中子数为( )
。该原子的原子核内中子数为( )