题目内容
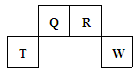
(8分)下表是元素周期表的一部分。表中所列的字母分别代表某一化学元素。
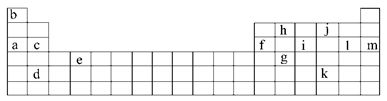
(1)下列__________(填写编号)组元素的单质具有良好导电性。
①a、c、h ②b、g、k ③c、h、i ④d、e、f
(2)下表是一些气态原子失去核外不同电子所需的能量,(即电离能,单位为kJ·mol-1):
①为什么锂原子的第二电离能远远大于第一电离能
________________________________________________________________________。
②表中X可能为以上13种元素中的__________(填写字母)元素。用元素符号表示X和j形成化合物的化学式_________________________________________________________。
③Y是周期表中__________族元素。
④以上13种元素中,_______(填写字母)元素原子失去核外第一个电子需要的能量最多。

(1)下列__________(填写编号)组元素的单质具有良好导电性。
①a、c、h ②b、g、k ③c、h、i ④d、e、f
(2)下表是一些气态原子失去核外不同电子所需的能量,(即电离能,单位为kJ·mol-1):
| 电离能 | 锂 | X | Y |
| I2 | 519 | 502 | 580 |
| I2 | 7 296 | 4 570 | 1 820 |
| I3 | 11 799 | 6 920 | 2 750 |
| I4 | | 9 550 | 11 600 |
________________________________________________________________________。
②表中X可能为以上13种元素中的__________(填写字母)元素。用元素符号表示X和j形成化合物的化学式_________________________________________________________。
③Y是周期表中__________族元素。
④以上13种元素中,_______(填写字母)元素原子失去核外第一个电子需要的能量最多。
(1)①④(2分) (2)①Li原子失去一个电子后,Li+已形成稳定结构,此时再失去一个电子很困难(1分) ②a(1分) Na2O和Na2O2(2分) ③ⅢA或第三主族(1分) ④m(1分)
(1)一般金属元素构成的单质具有很好的导电性,另外还原部分非金属元素的单质,例如石墨和硅等,所以答案是①④。
(2)锂失去1个电子后就达到了稳定结构,所以再失去电子是非常难的;X的第二电离能远大于第一电离能,说明X是第IA元素,又因为第一电离能小于锂的,所以应该是钠元素。J是氧。二者形成的氧化物是氧化钠和过氧化钠;Y的第一、第二和第三电离能逐渐增大,但相差不不是很大,而第四电离能则是远远的大于第一、第二和第三电离能,这说明Y是第ⅢA元素,即为铝元素;因为m是Ar,最外层电子已经达到稳定结构,所以第一电离能是最大的。
(2)锂失去1个电子后就达到了稳定结构,所以再失去电子是非常难的;X的第二电离能远大于第一电离能,说明X是第IA元素,又因为第一电离能小于锂的,所以应该是钠元素。J是氧。二者形成的氧化物是氧化钠和过氧化钠;Y的第一、第二和第三电离能逐渐增大,但相差不不是很大,而第四电离能则是远远的大于第一、第二和第三电离能,这说明Y是第ⅢA元素,即为铝元素;因为m是Ar,最外层电子已经达到稳定结构,所以第一电离能是最大的。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 B
B  C
C  D
D