题目内容
12.下列说法不正确的是( )①做一次中和热的测定,至少需要使用两次温度计.
②化石燃料在燃烧过程中能产生污染环境的CO、SO2等有害气体.
③铝热反应属于放热反应.
④同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H不同.
| A. | ①④ | B. | ②④ | C. | ②③ | D. | ③④ |
分析 ①根据温度计要测反应前酸溶液的温度,测反应前碱溶液的温度,混合反应后测最高温度一共3次;
②化石燃料在燃烧过程中,不完全燃烧会生成一氧化碳,含硫燃料煤燃烧易产生二氧化硫,产生的CO、S02等有害气体会污染环境;
③铝热反应是放热反应;
④反应的热效应只与始态、终态有关,与过程无关.
解答 解:①由于温度计要测反应前酸溶液的温度,测反应前碱溶液的温度,混合反应后测最高温度一共,所以完成一次测量至少使用3次温度计,故①错误;
②化石燃料在燃烧过程中产生的CO、S02等有害气体会污染环境,故②正确;
③铝热反应是金属铝和某些金属氧化物发生的放热反应,属于放热反应,故③正确;
④反应的热效应只与始态、终态有关,与过程无关,所以同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H相同,故④错误;
故选A.
点评 本题考查中和热、环境污染、反应热等,比较基础,注意对基础知识的理解掌握.

练习册系列答案
 巧学巧练系列答案
巧学巧练系列答案
相关题目
2.在0.1mol•L-1的Na2CO3溶液中,下列关系正确的是( )
| A. | c(Na+)=2c(CO32-) | B. | c(HCO3-)<c(H2CO3) | ||
| C. | c(Na+)<[c(CO32-)+c(HCO3-)] | D. | c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) |
3.在含0.2molKOH和0.1molBa(OH)2混合溶液中持续通入CO26.72L(标况)的过程中,溶液中离子的物质的量n和通入CO2体积V关系示意图正确的是( )
| A | B | C | D |
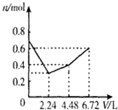 |  | 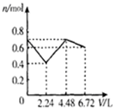 | 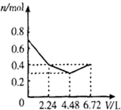 |
| A. | A | B. | B | C. | C | D. | D |
7.25℃,101kPa时,使1.0g钠与足量氯气反应,生成氯化钠晶体并放出17.87kJ的热量,生成1mo NaCl的反应热为( )
| A. | 17.87kJ | B. | -17.87kJ/mol | C. | 411 kJ/mol | D. | -411 kJ/mol |
17.下列说法正确的是( )
| A. | 置换反应一定属于氧化还原反应 | B. | 分解反应均不属于氧化还原反应 | ||
| C. | 复分解反应有的属于氧化还原反应 | D. | 化合反应有的属于氧化还原反应 |
4.钴的氧化物广泛应用于磁性材料及超导材料等领域.取一定量的钴的氧化物(其中钴的化合价为+2、+3价),用480mL 5mol•L-1盐酸恰好完全溶解固体,得到CoCl2溶液和4.48L(标准状况)黄绿色气体.通过计算可以确定该氧化物中Co、0的物质的量之比为( )
| A. | 1:1 | B. | 2:3 | C. | 3:4 | D. | 5:6 |
1.能说明Cl元素的非金属性比S元素的非金属性强的是( )
| A. | 含氧酸的酸性:HClO3强于H2SO4 | |
| B. | Cl元素的最高正价比S元素的最高正价要高 | |
| C. | 气态氢化物溶于水后的酸性:HCl比H2S强 | |
| D. | Cl2能与H2S水溶液反应,生成S单质 |
2.下列分散系中,分散质不能通过滤纸的是( )
| A. | 食盐水 | B. | 泥水 | C. | Fe(OH)3胶体 | D. | 硫酸铜溶液 |