��Ŀ����
�״�������һ������Դ���ȼ�ϣ�������Ϊ���͵������йط�Ӧ���Ȼ�ѧ����ʽ���£�
��2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)��H=-1275.6kJ/mol
��2CO(g)+O2(g)=2CO2(g)��H=-566.0kJ/mol
��H2O(g)= H2O(l)��H=-44kJ/mol
I.д��CH3OH(l)����ȫȼ������CO��H2O(l)���Ȼ�ѧ����ʽ��_________________��
II. ��ҵ�Ͽ���CO��H2��ȡ�״���CO(g)+2H2(g)=CH3OH(g) ��H=akJ/mol��Ϊ�о��÷�Ӧƽ��ʱCOת�����뷴Ӧ��Ͷ�ϱ�(��Ӧ��Ͷ�ϱ�=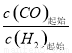 )�Լ��¶ȵĹ�ϵ���о�С����10L���ܱ������н���ģ�ⷴӦ��������Ӧ���ݻ����ͼ��
)�Լ��¶ȵĹ�ϵ���о�С����10L���ܱ������н���ģ�ⷴӦ��������Ӧ���ݻ����ͼ��
�ش��������⣺
��1����Ӧ��a____0(�>����<��)���ж�������______��
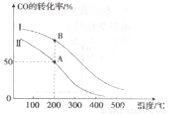
��2��������������ͬ������I��II�ֱ��ʾ��Ӧ��Ͷ�ϱȲ�ͬʱ�ķ�Ӧ�������ߡ�
�ٷ�Ӧ��Ͷ�ϱ�I_____II(�>����<�� ��=��)��
����������II��Ӧ��n(CO)��ʼ=10mol����Ӧ��Ͷ�ϱ�=0.5����A���ƽ�ⳣ��(Ka)ֵΪ____��B���ƽ�ⳣ��(Kb)ֵΪ________________��
��3��Ϊ���CO��ת���ʣ����˿����ʵ��ı䷴Ӧ�����������Ũ���⣬�����Բ�ȡ�Ĵ�ʩ�У�________________��_______________��