题目内容
【题目】下列离子组在一定条件下能大量共存,且加入相应试剂后所对应的离子方程式正确的是( )
选项 | 离子组 | 加入试剂 | 加入试剂后发生反应的离子方程式 |
A | Fe2+、NO | 稀H2SO4 | 3Fe2++NO |
B | Fe3+、I-、ClO- | NaOH溶液 | Fe3++3OH-=== Fe(OH)3↓ |
C | Mg2+、HCO | NaOH溶液 | HCO |
D | Al3+、Cl-、NO | 稀氨水 | Al3++3OH-=== Al(OH)3↓ |
A. A B. B C. C D. D
【答案】A
【解析】A.该组离子之间不反应,可大量共存,加稀硫酸发生3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,A正确;B.Fe3+、ClO-均能与I-发生氧化还原反应,不能大量共存,B错误;C.该组离子之间不反应,可大量共存,加NaOH发生Mg2++HCO3-+3OH-=Mg(OH)2↓+CO32-+H2O,C错误;D.该组离子之间不反应,可大量共存,加入稀氨水发生Al3++3NH3·H2O=Al(OH)3↓+3NH4+,D错误;答案选A。

 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案【题目】硫酸亚铁铵[(NH4)2Fe(SO4)2]是分析化学中的重要试剂,在不同温度下加热分解产物不同。设计如图实验装置(夹持装置略去),在500℃时隔绝空气加热A中的硫酸亚铁铵至分解完全,确定分解产物的成分。
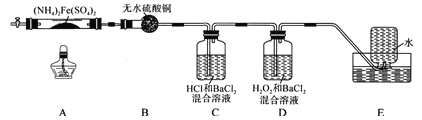
(1)B装置的作用是_________________________________________。
(2)实验中,观察到C中无明显现象,D中有白色沉淀生成,可确定产物中一定有____________气体产生,写出D中发生反应的离子方程式______________________。若去掉C,能否得出同样结论____________(填“是”或“否”) ,原因是____________________________。
(3)A中固体完全分解后变为红棕色粉末,某同学设计实验验证固体残留物仅为Fe2O3,而不含FeO,请帮他完成表中内容。(试剂,仪器和用品自选)
实验步骤 | 预期现象 | 结论 |
___________________________ | ________________________ | 固体残留物仅为Fe2O3 |
(4)若E中收集到的气体只有N2,其物质的量为xmol,固体残留物Fe2O3的物质的量为ymol,D中沉淀物质的量为zmol,则x、y和z应满足的关系为________________________。
(5)结合上述实验现象,完成硫酸亚铁铵在500℃时隔绝空气加热完全分解的化学方程式_______________。
