题目内容
密度为1.19g/cm3,质量分数为36.5%的浓盐酸100mL与二氧化锰加热充分反应,生成1.12L氯气(标准状况下).
求:
(1)该浓盐酸的物质的量浓度为多少?
(2)被氧化的HCl的物质的量为多少?
(3)在反应后溶液中加入足量AgNO3溶液,理论上可得多少克AgCl沉淀?(不考虑浓盐酸的挥发、氯气与水的反应)
解:(1)c=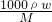 =
= =11.9mol/L,
=11.9mol/L,
答:该浓盐酸的物质的量浓度为11.9mol/L;
(2)n(Cl2)=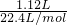 =0.05mol,则被氧化的HCl的物质的量为0.1mol,
=0.05mol,则被氧化的HCl的物质的量为0.1mol,
答:被氧化的HCl的物质的量为0.1mol;
(3)原溶液中含有n(Cl-)=11.9mol/L×0.1L=1.19mol,
被氧化的n(Cl-)=0.1mol,
则反应后溶液中剩余n(Cl-)=1.19mol-0.1mol=1.09mol,
所以能生成AgCl的物质的量为1.09mol,质量为1.09mol×143.5g/mol=156.4g,
答:理论上可得156.4gAgCl沉淀.
分析:(1)根据c=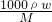 计算盐酸的物质的量浓度;
计算盐酸的物质的量浓度;
(2)根据生成的氯气的体积计算被氧化的HCl的物质的量;
(3)根据Cl元素守恒计算生成AgCl的质量.
点评:本题考查物质的量浓度、化学反应的相关计算,题目难度不大,答题时注意相关计算公式的运用.
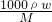 =
= =11.9mol/L,
=11.9mol/L,答:该浓盐酸的物质的量浓度为11.9mol/L;
(2)n(Cl2)=
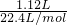 =0.05mol,则被氧化的HCl的物质的量为0.1mol,
=0.05mol,则被氧化的HCl的物质的量为0.1mol,答:被氧化的HCl的物质的量为0.1mol;
(3)原溶液中含有n(Cl-)=11.9mol/L×0.1L=1.19mol,
被氧化的n(Cl-)=0.1mol,
则反应后溶液中剩余n(Cl-)=1.19mol-0.1mol=1.09mol,
所以能生成AgCl的物质的量为1.09mol,质量为1.09mol×143.5g/mol=156.4g,
答:理论上可得156.4gAgCl沉淀.
分析:(1)根据c=
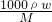 计算盐酸的物质的量浓度;
计算盐酸的物质的量浓度;(2)根据生成的氯气的体积计算被氧化的HCl的物质的量;
(3)根据Cl元素守恒计算生成AgCl的质量.
点评:本题考查物质的量浓度、化学反应的相关计算,题目难度不大,答题时注意相关计算公式的运用.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
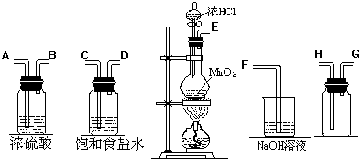
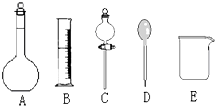 我校环保兴趣小组在处理污水样品时,需用质量分数为37%的浓盐酸(密度为1.19g/cm3)配制成250mL 0.1mol?L-1的盐酸溶液.
我校环保兴趣小组在处理污水样品时,需用质量分数为37%的浓盐酸(密度为1.19g/cm3)配制成250mL 0.1mol?L-1的盐酸溶液. 某环保兴趣小组在处理污水样品时,需用质量分数为36.5%的浓盐酸(密度为1.19g/cm3)配制成250mL0.1mol?L-1的盐酸溶液.
某环保兴趣小组在处理污水样品时,需用质量分数为36.5%的浓盐酸(密度为1.19g/cm3)配制成250mL0.1mol?L-1的盐酸溶液.