题目内容
19.已知硅能与碱反应产生氢气,将镁、铝、硅的混和物分为等质量的两份,一份跟足量的NaOH溶液反应,另一份跟足量的盐酸反应,最终产生的H2一样多.则镁与硅物质的量之比为( )| A. | 2:1 | B. | 4:1 | C. | 1:1 | D. | 3:1 |
分析 硅、铝与氢氧化钠反应生成氢气,铁不与氢氧化钠反应;Mg、铝与稀盐酸反应生成氢气,硅不与盐酸反应,两过程生成的氢气相等,反应中Al都表现+3价,铝与氢氧化钠、盐酸反应生成的氢气相等,则Mg与盐酸反应生成的氢气等于硅氢氧化钠反应生成的氢气,反应中Mg表现+2价、硅表现+4价,根据电子转移守恒计算铁与硅的物质的量之比.
解答 解:Si、Al与NaOH溶液反应生成氢气,Mg不与氢氧化钠反应,
Mg、Al与稀盐酸反应生成氢气,硅不与盐酸反应,两过程生成的氢气相等,反应中Al都表现+3价,铝与氢氧化钠、盐酸反应生成的氢气相等,则Mg与盐酸反应生成的氢气与硅、氢氧化钠反应生成的氢气的物质的量相等,
反应中Mg表现+2价、硅表现+4价,根据电子转移守恒有:
n(Mg)×2=n(Si)×4,
则:n(Mg):n(Si)=2:1,
故选A.
点评 本题考查混合物的有关计算,题目难度不大,明确发生反应及反应原理为解答关键,注意电子转移守在化学计算中的应用方法,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
9.下列物质与水混合后静置,不出现分层的是( )
| A. | 苯 | B. | 三氯甲烷 | C. | 乙酸 | D. | 四氯化碳 |
7.中科院国家纳米科学中心2013年11月22日宣布,该中心科研人员在国际上首次“拍”到氢键的“照片”,实现了氢键的实空间成像,为“氢键的本质”这一化学界争论了80多年的问题提供了直观证据.这不仅将人类对微观世界的认识向前推进了一大步,也为在分子、原子尺度上的研究提供了更精确的方法.下列说法中正确的是( )
| A. | 氢键是自然界中最重要、存在最广泛的化学键之一 | |
| B. | 正是氢键的存在,冰能浮在水面上 | |
| C. | 由于氢键的存在,沸点:HCl>HBr>HI>HF | |
| D. | 由于氢键的存在,水分子变的更稳定了 |
14.既能跟盐酸反应又能跟NaOH溶液反应的化合物是( )
| A. | Al | B. | Al2O3 | C. | Fe | D. | Fe2O3 |
4.下列各组元素最高价氧化物对应水化物碱性渐弱,酸性渐强的是( )
| A. | NaOH、Mg(OH)2、H3PO4、H2SO4 | B. | NaOH、KOH、H2SO4、HClO4 | ||
| C. | Be(OH)2、Ca(OH)2、HBrO4、HClO4 | D. | Mg(OH)2、Ba(OH)2、H3PO4、H2SO4 |
11.自来水可用氯气消毒,用这种自来水配制下列物质溶液,不会产生明显的药品变质问题的是( )
| A. | AgNO3溶液 | B. | NaCl | C. | FeCl2 | D. | NaOH |
8.在下列无色透明溶液中,能大量共存的离子组是( )
| A. | Cu2+、Na+、SO42-、Cl- | B. | Ca2+、NH4+、Cl-、OH- | ||
| C. | Ba2+、H+、I-、SO42- | D. | Mg2+、Na+、NH4+、NO3- |
9.下列有关叙述正确的是( )
| A. | H、D、T具有相同的质子数,是氢元素的三种同位素 | |
| B. | OH-与H3O+组成元素相同,所含质子数相同 | |
| C. | 结构示意图为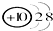 和 和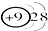 两种粒子为同一种元素 两种粒子为同一种元素 | |
| D. | 元素原子最外层电子数的多少是判断金属性和非金属性强弱的依据 |