题目内容
某无色溶液中可能含有:Na+、Ba2+、Cu2+、CO32-、Cl-、Mg2+.
①:向此溶液中滴加稀HCl无明显现象.
②:取少许①的溶液并加入少量的Na2SO4溶液,有白色沉淀产生.
③:取②的上层清液并加入过量的NaOH溶液,无明显的现象.请回答下列问题:
(1)原溶液中一定含有的离子是
(2)②中的离子方程式是
①:向此溶液中滴加稀HCl无明显现象.
②:取少许①的溶液并加入少量的Na2SO4溶液,有白色沉淀产生.
③:取②的上层清液并加入过量的NaOH溶液,无明显的现象.请回答下列问题:
(1)原溶液中一定含有的离子是
Ba2+、Cl-
Ba2+、Cl-
,一定不含的离子是CO32-、Mg2+、Cu2+
CO32-、Mg2+、Cu2+
,不能确定是否含有的离子是Na+
Na+
.(2)②中的离子方程式是
Ba2++SO42-=BaSO4↓
Ba2++SO42-=BaSO4↓
.分析:向此溶液中滴加稀HCl无明显现象,说明溶液中不存在CO32-;
根据溶液电中性原则,则一定含有Cl-;
溶液无色,则一定不含Cu2+;
取少许①的溶液并加入少量的Na2SO4溶液,有白色沉淀产生,则溶液中含有Ba2+;
取②的上层清液并加入过量的NaOH溶液,无明显的现象,说明不含Mg2+.
以此解答该题.
根据溶液电中性原则,则一定含有Cl-;
溶液无色,则一定不含Cu2+;
取少许①的溶液并加入少量的Na2SO4溶液,有白色沉淀产生,则溶液中含有Ba2+;
取②的上层清液并加入过量的NaOH溶液,无明显的现象,说明不含Mg2+.
以此解答该题.
解答:解:(1)向此溶液中滴加稀HCl无明显现象,说明溶液中不存在CO32-;
根据溶液电中性原则,则一定含有Cl-;
溶液无色,则一定不含Cu2+;
取少许①的溶液并加入少量的Na2SO4溶液,有白色沉淀产生,则溶液中含有Ba2+;
取②的上层清液并加入过量的NaOH溶液,无明显的现象,说明不含Mg2+.
应没有涉及到Na+的性质实验,则不能确定Na+离子是否存在,
故答案为:Ba2+、Cl-;CO32-、Mg2+、Cu2+;Na+;
(2)取少许①的溶液并加入少量的Na2SO4溶液,有白色沉淀产生,该沉淀为BaSO4,发生的反应为Ba2++SO42-=BaSO4↓,
故答案为:Ba2++SO42-=BaSO4↓.
根据溶液电中性原则,则一定含有Cl-;
溶液无色,则一定不含Cu2+;
取少许①的溶液并加入少量的Na2SO4溶液,有白色沉淀产生,则溶液中含有Ba2+;
取②的上层清液并加入过量的NaOH溶液,无明显的现象,说明不含Mg2+.
应没有涉及到Na+的性质实验,则不能确定Na+离子是否存在,
故答案为:Ba2+、Cl-;CO32-、Mg2+、Cu2+;Na+;
(2)取少许①的溶液并加入少量的Na2SO4溶液,有白色沉淀产生,该沉淀为BaSO4,发生的反应为Ba2++SO42-=BaSO4↓,
故答案为:Ba2++SO42-=BaSO4↓.
点评:本题考查离子的检验和推断,题目难度中等,注意把握离子反应的实验现象以及离子的检验的实验操作方法.

练习册系列答案
相关题目
(2011?河西区一模)某无色溶液中可能含有 ①Na+、②Ba2+、③Cl-、④Br-、⑤SO42-、⑥SO32-离子中的若干种,依顺序进行下列实验,且每步所加试剂均过量,观察到的现象如下:
|
某无色溶液中可能含有I-、NH4+、Cu2+、SO32-,向该溶液中加入少量溴水,溶液呈无色,则下列关于溶液组成的判断正确的是( )
①肯定不含I- ②肯定不含Cu2+ ③肯定含有SO32-④可能含有I-.
①肯定不含I- ②肯定不含Cu2+ ③肯定含有SO32-④可能含有I-.
| A、①③ | B、①②③ | C、③④ | D、②③④ |
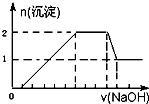 某无色溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-等离子中的几种,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示.下列说法一定正确的是( )
某无色溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42-等离子中的几种,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示.下列说法一定正确的是( )| A、一定存在H+、Mg2+、Al3+、NH4+,一定不存在Na+、SO42-、Fe3+ | B、一定存在H+、Al3+、NH4+、SO42-,可能存在Na+、Mg2+ | C、溶液中c(H+):c(Al3+):c(Mg2+)为1:1:1 | D、溶液中c(H+):c(SO42-)为2:9 |