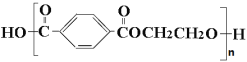题目内容
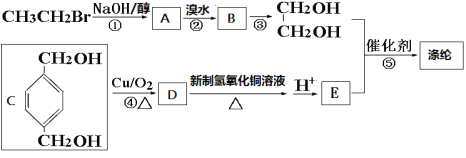
【题目】工业废气、汽车尾气排放出的SO2、NOx等,是形成雾霾的重要因素。霾是由空气中的灰尘、硫酸、硝酸、有机碳氢化合物等粒子形成的烟雾。
(1)NOx和SO2在空气中存在下列平衡:
2NO(g)+ O2(g)![]() 2NO2(g) △H= —112 kJ·mol-1
2NO2(g) △H= —112 kJ·mol-1
2SO2(g)+ O2 (g) ![]() 2SO3(g) △H= —196 kJ·mol-1
2SO3(g) △H= —196 kJ·mol-1
SO2通常被NO2进一步氧化,生成SO3和一种无色有毒的气体。请写出NO2和SO2反应的热化学方程式______________。
(2) 常温下,烟气中SO2被NaOH溶液吸收可得到NaHSO3、Na2SO3等。
①已知Na2SO3水溶液显碱性,原因是____________(写出主要反应的离子方程式),该溶液中c(Na+)____ 2c(SO32-)+ c(HSO3-)(填“>”“<”或“=”)。
②常温下,0.1mol/L的NaHSO3溶液的PH=6,则c(SO32-)—c(H2SO3)= ______ mol/L(填写准确数值)。
【答案】NO2(g)+SO2(g)![]() SO3(g)+ NO(g) △H= —42 kJ/mol SO32- + H2O
SO3(g)+ NO(g) △H= —42 kJ/mol SO32- + H2O![]() HSO3-+ OH- > ②9.9×10-7
HSO3-+ OH- > ②9.9×10-7
【解析】
(1)已知:①2NO(g)+O2(g)2NO2(g)△H=-112kJmol-1,②2SO2(g)+O2(g)2SO3(g)△H=-196kJmol-1,根据盖斯定律可知(②-①)÷2得:NO2(g)+SO2(g)=SO3(g)+NO(g),则可计算△H;
(2)①溶液中SO32-水解:SO32-+H2OHSO3-+OH-,破坏水的电离平衡,导致溶液显碱性,根据电荷守恒分析;
②常温下,亚硫酸氢钠呈酸性,说明亚硫酸氢根离子的电离程度大于水解程度,根据物料守恒得c(Na+)=c(H2SO3)+c(HSO3-)+c(SO32-)①,根据电荷守恒得c(Na+)+c(H+)=c(OH-)+c(HSO3-)+2c(SO32-)②,两式计算得到。
(1)已知:①2NO(g)+O2(g)2NO2(g)△H=-112kJmol-1,②2SO2(g)+O2(g)2SO3(g)△H=-196kJmol-1,根据盖斯定律可知(②-①)÷2得:NO2(g)+SO2(g)=SO3(g)+NO(g),则△H=[(-196kJmol-1)-( -112kJmol-1)]÷2==-42kJmol-1,故NO2和SO2反应的热化学方程式为:NO2(g)+SO2(g)=SO3(g)+NO(g)△H=-42 kJmol-1;
(2)①溶液中SO32-水解:SO32-+H2OHSO3-+OH-,破坏水的电离平衡,导致溶液显碱性,根据电荷守恒,溶液中c(H+)+c(Na+)=2c(SO32-)+c(HSO3-)+c(OH-),故c(Na+)<2c(SO32-)+c(HSO3-)+c(OH-);
②常温下,亚硫酸氢钠呈酸性,说明亚硫酸氢根离子的电离程度大于水解程度,根据物料守恒得c(Na+)=c(H2SO3)+c(HSO3-)+c(SO32-)①,根据电荷守恒得c(Na+)+c(H+)=c(OH-)+c(HSO3-)+2c(SO32-)②,将方程式①代入②得,c(H2SO3)+c(H+)=c(OH-)+c(SO32-),所以c(SO32-)-c(H2SO3)=c(H+)-c(OH-)=(10-6-10-8)molL-1=9.9×10-7molL-1。

 阅读快车系列答案
阅读快车系列答案【题目】下列“实验结论”与“实验操作及现象”不相符的一组是
选项 | 实验操作及现象 | 实验结论 |
A | 向KI―淀粉溶液中滴加氯水,溶液变成蓝色 | 氧化性:Cl2>I2 |
B | 向蔗糖中滴加浓硫酸,蔗糖变黑 | 浓硫酸有吸水性 |
C | 向某盐溶液中滴加KSCN溶液,溶液变为红色 | 该溶液中含有Fe3+ |
D | 向某盐溶液中加入浓NaOH溶液,加热,产生的气体能使湿润的红色石蕊试纸变蓝 | 该溶液中含有 |
A.AB.BC.CD.D