题目内容
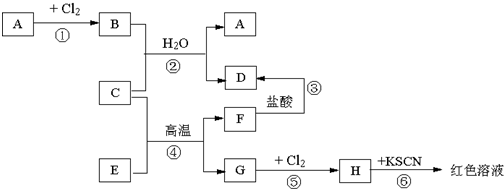
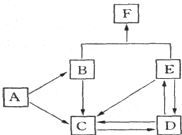
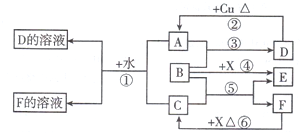
A~F是中学化学中常见物质,常温下A、C、E、F为气体,B、D为液体,其中B的分子为4原子分子,D在常温下不具有挥发性.F的浓溶液与X共热通常用于实验室制备单质C,X是一种黑色粉末.这些物质之间满足如下图所示的转化关系,图中部分生成物已略去.
(1)写出下列物质的化学式:A______,F______.
(2)B的电子式是______.根据图中信息,B、C、X的氧化性由强到弱的顺序是______(用化学式表示).
(3)反应⑥的离子方程式是______.
(4)在反应⑥中,F表现的性质是______,当生成0.75molC时,被氧化的还原剂的物质的量是______.

(1)写出下列物质的化学式:A______,F______.
(2)B的电子式是______.根据图中信息,B、C、X的氧化性由强到弱的顺序是______(用化学式表示).
(3)反应⑥的离子方程式是______.
(4)在反应⑥中,F表现的性质是______,当生成0.75molC时,被氧化的还原剂的物质的量是______.
B、D为液体,其中B的分子为4原子分子,因此B是H2O2,D在常温下不具有挥发性,且D能和铜反应,这说明D应该是H2SO4,则根据A是气体可知A是SO2,F的浓溶液与X共热通常用于实验室制备单质C,且C、E、F为气体,由于H2O2易分解生成O2,这说明E应该是O2,则X就是MnO2,所以C是Cl2,F是HCl,
(1)由以上分析可知A为SO2,F为HCl,故答案为:SO2;HCl;
(2)B是H2O2,为共价化合物,电子式为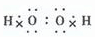 ,根据氧化还原反应中氧化剂的氧化性强于氧化产物的可知,B、C、X的氧化性由强到弱的顺序是MnO2>Cl2>H2O2,故答案为:
,根据氧化还原反应中氧化剂的氧化性强于氧化产物的可知,B、C、X的氧化性由强到弱的顺序是MnO2>Cl2>H2O2,故答案为: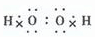 ;MnO2>Cl2>H2O2;
;MnO2>Cl2>H2O2;
(3)反应⑥是实验室制取氯气,反应的离子方程式是MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O,故答案为:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O;
(4)在实验室制取氯气的反应中,浓盐酸表现出的性质是还原性和酸性.根据氯原子守恒可知,当生成0.75mol 氯气时,被氧化的还原剂的物质的量是0.75mol×2=1.5mol,
故答案为:还原性、酸性;1.5mol.
(1)由以上分析可知A为SO2,F为HCl,故答案为:SO2;HCl;
(2)B是H2O2,为共价化合物,电子式为
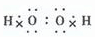 ,根据氧化还原反应中氧化剂的氧化性强于氧化产物的可知,B、C、X的氧化性由强到弱的顺序是MnO2>Cl2>H2O2,故答案为:
,根据氧化还原反应中氧化剂的氧化性强于氧化产物的可知,B、C、X的氧化性由强到弱的顺序是MnO2>Cl2>H2O2,故答案为: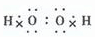 ;MnO2>Cl2>H2O2;
;MnO2>Cl2>H2O2;(3)反应⑥是实验室制取氯气,反应的离子方程式是MnO2+4H++2Cl-
| ||
| ||
(4)在实验室制取氯气的反应中,浓盐酸表现出的性质是还原性和酸性.根据氯原子守恒可知,当生成0.75mol 氯气时,被氧化的还原剂的物质的量是0.75mol×2=1.5mol,
故答案为:还原性、酸性;1.5mol.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目