题目内容
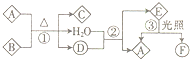
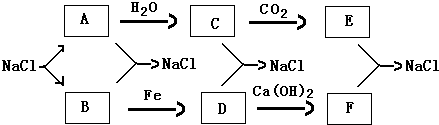
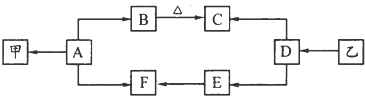
图中A是现代社会中用量最多的金属,F为红褐色沉淀.请根据如图所示的转化关系回答下列问题:

(1)分别写出反应①、反应③的化学方程式:______;______.
(2)写出反应②的离子方程式:______.

(1)分别写出反应①、反应③的化学方程式:______;______.
(2)写出反应②的离子方程式:______.
A是现代社会中用量最多的金属,则A是铁,F为红褐色沉淀,则F是氢氧化铁,E被氧化生成氢氧化铁,则E是氢氧化亚铁,D和氢氧化钠溶液生成氯化钠和氢氧化铁,根据元素守恒知,D是氯化铁,C和氢氧化钠反应生成氯化钠和氢氧化亚铁,则C是氯化亚铁,铁和水蒸气反应生成四氧化三铁和氢气,铁和盐酸反应生成氯化亚铁和氢气,所以G是氢气,B是四氧化三铁,
(1)高温条件下,铁和水蒸气反应生成四氧化三铁和氢气,反应方程式为:3Fe+4H2O(g)
Fe3O4+4H2,氢氧化亚铁不稳定,易被氧气氧化生成氢氧化铁,反应方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,
故答案为:3Fe+4H2O(g)
Fe3O4+4H2;4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(2)亚铁离子具有还原性,氯气具有强氧化性,所以氯气能氧化亚铁离子生成铁离子,自身被还原生成氯离子,离子反应方程式为2Fe2++Cl2=2Fe3++2Cl-,
故答案为:2Fe2++Cl2=2Fe3++2Cl-.
(1)高温条件下,铁和水蒸气反应生成四氧化三铁和氢气,反应方程式为:3Fe+4H2O(g)
| ||
故答案为:3Fe+4H2O(g)
| ||
(2)亚铁离子具有还原性,氯气具有强氧化性,所以氯气能氧化亚铁离子生成铁离子,自身被还原生成氯离子,离子反应方程式为2Fe2++Cl2=2Fe3++2Cl-,
故答案为:2Fe2++Cl2=2Fe3++2Cl-.

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目