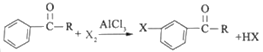题目内容
【题目】德国化学家凯库勒认为:苯分子是由6个碳原子以单双键相互交替结合而成的环状结构为了验证凯库勒有关苯环的观点,甲同学设计了如图实验方案.

①按如图所示的装置图连接好各仪器;②检验装置的气密性;③在A中加入适量的苯和液溴的混合液体,再加入少量铁粉,塞上橡皮塞,打开止水夹K1、K2、K3;④待C中烧瓶收集满气体后,将导管b的下端插入烧杯里的水中,挤压預先装有水的胶头滴管的胶头,观察实验现象.
请回答下列问题.
(1)A中所发生反应的反应方程式为_____,能证明凯库勒观点错误的实验现象是______.
(2)装置B的作用是______.
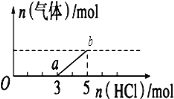
(3)C中烧瓶的容积为500mL,收集气体时,由于空气未排尽,最终水未充满烧瓶,假设烧瓶中混合气体对氢气的相对密度为35.3,则实验结束时,进入烧瓶中的水的体积为______mL 空气的平均相对分子质量为29.
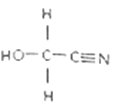
(4)已知乳酸的结构简式为![]() 试回答:
试回答:
①乳酸分子中含有______和______两种官能团写名称.
②乳酸跟氢氧化钠溶液反应的化学方程式:______.
【答案】.![]() ; 烧瓶中产生“喷泉”现象 除去未反应的苯蒸气和溴蒸气 400 羟基 羧基 CH3CH(OH)COOH+NaOH→CH3CH(OH)COONa+H2O
; 烧瓶中产生“喷泉”现象 除去未反应的苯蒸气和溴蒸气 400 羟基 羧基 CH3CH(OH)COOH+NaOH→CH3CH(OH)COONa+H2O
【解析】
(1)苯与溴在溴化铁做催化剂的条件下生成溴苯和溴化氢,苯分子里的氢原子被溴原子所代替,
方程式为:![]() ,该反应为取代反应,不是加成反应,所以苯分子中不存在碳碳单双键交替,所以凯库勒观点错误,生成的溴化氢极易溶于水,所以C中产生“喷泉”现象;
,该反应为取代反应,不是加成反应,所以苯分子中不存在碳碳单双键交替,所以凯库勒观点错误,生成的溴化氢极易溶于水,所以C中产生“喷泉”现象;
(2)因为反应放热,苯和液溴均易挥发,苯和溴极易溶于四氯化碳,用四氯化碳除去溴化氢气体中的溴蒸气和苯,以防干扰检验HBr;
(3)烧瓶中混合气体对氢气的相对密度为35.3,故烧瓶中混合气体的平均分子量为35.3×2=70.6,
设HBr的体积为x,空气的体积为y,则:81×x/500+29×y/500=70.6;x+y=500,计算得出:x=400mL,y=100mL,所以进入烧瓶中的水的体积为400mL;
(4)①乳酸分子中含羟基(-OH)和羧基(-COOH);
②羧基与氢氧根发生中和反应,反应方程式为:CH3CH(OH)COOH+NaOH→CH3CH(OH)COONa+H2O。