题目内容
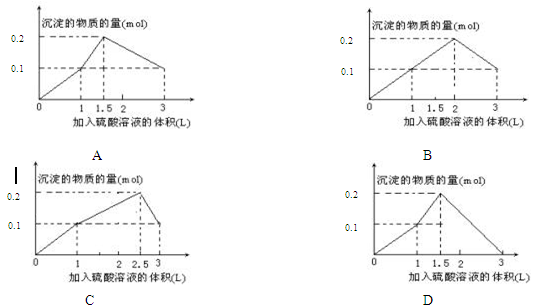
将2.7g Al与100mL 2 mol/L H2SO4溶液充分反应后,再慢慢滴入25mL 4mol/LNaOH溶液,其结果是:( )
| A.所得溶液的pH<7 |
| B.溶液中有较多Al(OH)3沉淀 |
| C.取少量所得溶液,加NaHCO3,无明显现象发生 |
| D.另取少量所得溶液,加入几滴浓NaOH溶液,无明显变化 |
A
涉及反应(铝为0.1mol、H+为0.4mol、滴入的OH-为0.1mol):
2Al+6H+=2Al3++3H2↑ H++OH-=H2O
0.1 0.3 0.1 0.1 0.1
可见,铝可消耗0.3mol的H+,剩余的0.1molH+与OH-恰好中和,最终溶液中含有的离子有:Al3+、Na+、SO42-
A:由于Al3+的水解,溶液呈酸性,pH小于7,正确
B:无沉淀
C:Al3++3HCO3-=Al(OH)3↓+3CO2↑,发生又水解反应,有沉淀与气体生成
D:Al3+将与OH—生成白色沉淀,不正确
答案为A
2Al+6H+=2Al3++3H2↑ H++OH-=H2O
0.1 0.3 0.1 0.1 0.1
可见,铝可消耗0.3mol的H+,剩余的0.1molH+与OH-恰好中和,最终溶液中含有的离子有:Al3+、Na+、SO42-
A:由于Al3+的水解,溶液呈酸性,pH小于7,正确
B:无沉淀
C:Al3++3HCO3-=Al(OH)3↓+3CO2↑,发生又水解反应,有沉淀与气体生成
D:Al3+将与OH—生成白色沉淀,不正确
答案为A

练习册系列答案
相关题目