题目内容
在2L密闭容器中发生3X(g)+Y(g) 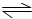 Z (g)+2W(g)反应,现在控制下列三种不同的条件:
Z (g)+2W(g)反应,现在控制下列三种不同的条件:
①在400°C时,9mol X 与3mol Y 反应
②在400°C时,15mol X 与5mol Y 反应
③在300°C 时,9mol X 与3mol Y 反应
那么,(1)反应开始时,正反应速率最大的是(填序号,下同)
(2)在①条件下的反应进行到第10min时,测得Z为1mol,此时v(Z)=
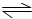 Z (g)+2W(g)反应,现在控制下列三种不同的条件:
Z (g)+2W(g)反应,现在控制下列三种不同的条件:①在400°C时,9mol X 与3mol Y 反应
②在400°C时,15mol X 与5mol Y 反应
③在300°C 时,9mol X 与3mol Y 反应
那么,(1)反应开始时,正反应速率最大的是(填序号,下同)
②
②
,正反应速率最小的是③
③
;(2)在①条件下的反应进行到第10min时,测得Z为1mol,此时v(Z)=
0.05
0.05
mol/(L?min);v(X)=0.15
0.15
mol/(L?min).分析:(1)根据温度、浓度对化学反应速率的影响来解题;
(2)根据V=
=
求出Z的反应速率,根据化学反应速率之比等于化学计量数之比求出X的反应速率;
(2)根据V=
| △C |
| △t |
| ||
| △t |
解答:解:(1)因其他条件相同时,温度越高,化学反应速率越大,故①>③;其他条件相同时,反应物的浓度越大,化学反应速率越大,故②>①;故答案为:②;③;
(2)根据V(Z)=
=
=
=0.05mol/(L?min),v(X)=3V(Z)=0.15mol/(L?min),
故答案为:0.05;0.15.
(2)根据V(Z)=
| △C |
| △t |
| ||
| △t |
| ||
| 10min |
故答案为:0.05;0.15.
点评:本题主要考查了影响化学反应速率的因素、化学反应速率的计算,需要注意的是化学反应速率之比等于化学计量数之比.

练习册系列答案
相关题目
(2013?浦东新区三模)一定温度下,在2L密闭容器中发生下列反应:4NO2(g)+O2(g)?2N2O5(g);已知该反应的平衡常数:k300℃>k350℃,且体系中n(NO2)(单位:mol)随时间变化如下表:
|
一定条件下,使X(g)与Y(g)在2L密闭容器中发生反应生成z(g).温度为TK时,反应过程中X,Y,Z的物质的量变化如图1所示;若保持其他条件不变,温度分别为T,K和T2,K时,Y的体积分数与时间的关系如图2所示.则下列结论正确的是( )
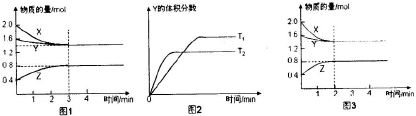

| A、反应进行的前3min内,用X表示的反应速率V(X)=0.1mol/(L?min) | B、平衡时容器内的压强为反应前的0.8倍 | C、保持其他条件不变,升高温度,反应的化学平衡常数K减小 | D、若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强 |
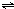 ClO(g)+3H2(g)△H>0.
ClO(g)+3H2(g)△H>0. CH3OH(g)△H=-90.1kJ?mol-1,恒容条件下达平衡,下列措施中能使n(CH3OH)/n(CO)增大的有
CH3OH(g)△H=-90.1kJ?mol-1,恒容条件下达平衡,下列措施中能使n(CH3OH)/n(CO)增大的有
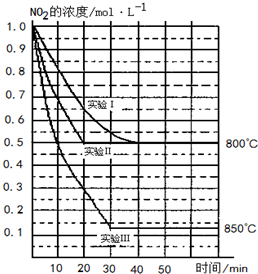 某条件下,在2L密闭容器中发生如下反应2NO2(g)?2NO(g)+O2(g)
某条件下,在2L密闭容器中发生如下反应2NO2(g)?2NO(g)+O2(g)