题目内容
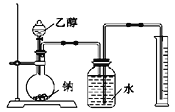
【题目】实验需要0.1mol/LNaCl溶液450ml,根据溶液配制中情况回答下列问题:
(1)实验中除了托盘天平、烧杯、容量瓶、玻璃棒外还需要的仪器是____。
(2)根据计算得知,所需NaCl的质量为____g。
(3)所选容量瓶的规格是____。(填字母)
A.50mL的容量瓶 B.150mL的容量瓶
C.250mL的容量瓶 D.500mL的容量瓶
(4)下列操作对所配浓度的影响:偏大的有___;(填写字母)偏小的有___;无影响的有__。
A.称量用了生锈的砝码; B.往容量瓶转移时,有少量液体溅出;
C.未洗涤溶解NaCl的烧杯; D.容量瓶未干燥即用来配制溶液;
E.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线。
【答案】胶头滴管 2.9g D A BCE D
【解析】
(1)根据配制溶液的实验操作过程选择所用仪器;
(2)根据n=cV计算氯化钠的物质的量,再根据m=nM计算所需氯化钠的质量;
(3)根据“大而近”的原则,根据需要配制溶液的体积来选择合适的容量瓶;
(4)分析操作对溶质的物质的量或对溶液的体积的影响,根据c=![]() 分析判断。
分析判断。
(1)没有450mL规格容量瓶,所以选用500mL容量瓶;操作步骤有计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解(可用量筒量取水加入烧杯),并用玻璃棒搅拌,加速溶解,冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2~3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.所以所需仪器有托盘天平、烧杯、玻璃棒、500mL容量瓶、胶头滴管、药匙;根据提供的仪器可知,还需仪器有胶头滴管;
(2)氯化钠的质量为m=0.5L×0.1molL-1×58.5g/mol=2.925g,则所需NaCl的质量为2.9g;
(3)没有450mL规格容量瓶,所以选用500mL容量瓶,故答案为D;
(4)A.称量用了生锈的砝码,所称NaCl的质量偏高,则配制溶液浓度偏大;
B.往容量瓶转移时,有少量液体溅出,容量瓶内NaCl的质量偏低,则配制溶液浓度偏小;
C.未洗涤溶解NaCl的烧杯,烧杯内有残余NaCl,容量瓶内NaCl的质量偏低,则配制溶液浓度偏小;
D.容量瓶未干燥即用来配制溶液,不影响容量瓶内NaCl的质量和溶液的体积,对所配溶液的体积无影响;
E.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线,导致溶液体积偏大,配制溶液浓度偏小;
故:所配浓度偏大的有A;偏小的有BCE;无影响的有D。

 阅读快车系列答案
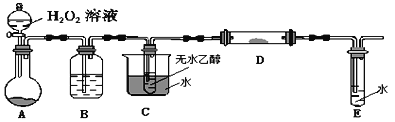
阅读快车系列答案【题目】为验证氧化性Cl2 > Fe3+> SO2,某小组用下图所示装置进行实验(夹持仪器和A中加热装置已略)。

实验过程:
Ⅰ.查好装置的气密性后,在各仪器中添加相应试剂
Ⅱ.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4
Ⅲ.打开活塞a,滴加一定量的浓盐酸,给A加热
Ⅳ.当B中溶液变黄时,停止加热,关闭K2
Ⅴ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
Ⅵ.打开K3和活塞c,加入70%的硫酸,一段时间后关闭K3
VII. 更换试管D,重复过程V,检验B溶液中的离子
(1)检验虚线框内装置气密性的操作是____。
(2)B棉花中浸润的溶液为____。实验Ⅱ通入N2的作用是____。
(3)C中发生反应的化学方程式_____。
(4)用70%的硫酸制取SO2,反应速率比用98%的硫酸快,原因是____。
(5)若将制取的SO2通入酸性高锰酸钾溶液可使溶液褪色,其离子方程式为___。
(6)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示。他们的检测结果一定能够证明氧化性Cl2 > Fe3+>SO2的是___(填“甲”“乙”“丙”)。
过程ⅣB溶液中含有的离子 | 过程ⅥB溶液中含有的离子 | |
甲 | 既有Fe3+又有Fe2+ | 有SO42- |
乙 | 有Fe3+无Fe2+ | 有SO42- |
丙 | 有Fe3+无Fe2+ | 有Fe2+ |