题目内容
下列事实与浓硫酸表现出的性质(括号中)对应关系正确的是( )
| A.在空气中敞口久置的浓硫酸,溶液质量增大(脱水性) |
| B.在加热条件下铜与浓硫酸反应(氧化性、酸性) |
| C.蔗糖与浓硫酸反应中有海棉状的炭生成(吸水性) |
| D.浓硫酸可用来干燥某些气体(不挥发性) |
B
解析试题分析:A、在空气中敞口久置的浓硫酸,会吸收空气中的水分而使溶液的质量增大,表现的是浓硫酸的吸水性,错误;B、在加热条件下铜与浓硫酸反应发生氧化还原反应2H2SO4(浓)+Cu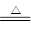 CuSO4+SO2↑+2H2O,表现的是浓硫酸的氧化性和酸性,正确;C、浓硫酸能使有机物中的H、O元素以水的形式脱出,则蔗糖与浓硫酸反应中有海棉状的炭生成,表现的是浓硫酸的脱水性,错误;D、浓硫酸可以用来干燥某些与浓硫酸不反应的气体,表现的是浓硫酸的吸水性,错误。
CuSO4+SO2↑+2H2O,表现的是浓硫酸的氧化性和酸性,正确;C、浓硫酸能使有机物中的H、O元素以水的形式脱出,则蔗糖与浓硫酸反应中有海棉状的炭生成,表现的是浓硫酸的脱水性,错误;D、浓硫酸可以用来干燥某些与浓硫酸不反应的气体,表现的是浓硫酸的吸水性,错误。
考点:考查浓硫酸的性质。

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
氯水中存在多种分子和离子,可通过实验的方法加以确定。下列有关氯水中存在粒子的说法正确的是( )
| A.加入有色布条,一会儿有色布条褪色,证明有Cl2存在 |
| B.溶液呈黄绿色,且有刺激性气味,证明有Cl2分子存在 |
| C.先加入盐酸酸化,再加入AgNO3溶液,产生白色沉淀,证明有Cl-存在 |
| D.加入NaOH溶液,氯水黄绿色消失,证明有HClO分子存在 |
将一定质量的铜粉加入到100mL,某浓度的稀硝酸中充分反应后,容器中剩有m1g铜粉,此时共收集到NO气体336mL(标准状况) 。然后向上述混合物中加入稀硫酸至不再反应为止容器剩有铜粉m2g,则m1-m2为( )
| A.5.76 | B.2.88 | C.1.44 | D.4.32 |
现有甲、乙、丙三瓶等体积的新制氯水,浓度均为0.1 mol/L,,如果在甲瓶中加入少量的NaHCO3晶体,在乙瓶中加入少量的NaHSO3晶体,丙瓶不变。片刻后,甲、乙、丙三瓶溶液中HClO的物质的量浓度的大小关系为(忽略溶液体积变化) ( )
| A.甲=乙>丙 | B.甲>丙>乙 | C.丙>甲=乙 | D.乙>丙>甲 |
某同学用下列装置制备并检验Cl2的性质。下列说法正确的是
| A.实验室制氯气中除去尾气用澄清石灰水 |
| B.吸收了氯气的NaOH溶液中滴入硫酸,至溶液显酸性,结果有Cl2生成 |
| C.铜丝在氯气中燃烧生成蓝色的烟 |
| D.甲烷和氯气的混合气体中发生了加成反应 |
不论以何种比例混合,将甲和乙两种混合气体同时通入过量的丙溶液中,一定能产生沉淀的组合是
| 序号 | 甲 | 乙 | 丙 |
| ① | CO2 | SO2 | 石灰水 |
| ② | HCl | CO2 | 石灰水 |
| ③ | CO2 | SO2 | Ba(NO3)2 |
| ④ | NO2 | SO2 | BaCl2 |
| ⑤ | CO2 | NH3 | CaCl2 |
向含有NaBr 、KI的混合溶液中通入过量的Cl2充分反应。将溶液蒸干并灼烧,最后剩余的固体物质是( )
| A.NaCl 和KI | B.NaCl、KCl和I2 | C.KCl和NaBr | D.KCl和NaCl |
某实验过程如图所示,则图③试管中的现象是
| A.铜片溶解、产生无色气休,该气体遇空气变为红棕色 |
| B.铜片溶解.产生无色气体,该气体遇到空气不变色 |
| C.铜片溶解,放出红棕色有刺激性气味的气体 |
| D.无明显现象。因稀硫酸不与铜反应 |
下表实验中“操作及现象”与“给定溶液”的性质不对应的是
| 选项 | 溶液 | 操作及现象 |
| A | Ca(OH)2溶液 | 通入CO2,溶液变浑浊。继续通CO2至过量,浑浊消失。再加入足量NaOH溶液,又变浑浊。 |
| B | 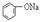 溶液 溶液 | 通入CO2,溶液变浑浊。继续通CO2至过量,浑浊消失。 |
| C | Ca(ClO)2溶液 | 通入CO2,溶液没有明显变化。再滴入品红溶液,红色褪去。 |
| D | CaCl2溶液 | 通入CO2,溶液没有明显变化。若同时通入CO2和NH3,则溶液变浑浊。 |