题目内容
3.下列物质①氯水;②氨气;③氢氧化钠溶液;④氯化钠晶体;⑤蔗糖;⑥醋酸;⑦硫酸钡;⑧酒精;⑨熔化的KNO3;⑩铁,(填序号)(1)以上物质能导电的是①③⑨⑩;
(2)以上物质属于强电解质的是④⑦⑨;
(3)以上物质属于弱电解质的是⑥;
(4)以上物质属于非电解质的是②⑤⑧.
分析 在水溶液或熔融状态下能够导电的化合物为电解质,在水溶液和熔融状态下都不能导电的化合物为非电解质;在水溶液中能够完全电离的化合物为强电解质,部分电离的为弱电解质;单质和混合物既不是电解质,也不是非电解质,物质导电的条件是存在自由电子或者自由移动的离子,
据此进行判断.
解答 解:①氯水是混合物,不是电解质也不是非电解质,含有氢离子、氯离子等,能够导电;
②氨气本身不能电离产生自由移动的离子,属于非电解质,不导电;
③氢氧化钠溶液,属于混合物,不是电解质也不是非电解质,含有钠离子、氢氧根离子,能够导电;
④氯化钠晶体,在水溶液或熔融状态下能够完全电离产生自由移动离子,属于强电解质,不含自由移动的离子,不导电;
⑤蔗糖在水溶液和熔融状态下都不能导电的化合物,是非电解质,不导电;
⑥醋酸在水溶液中能够部分电离产生自由移动离子,属于弱电解质,不含自由移动的离子,不导电;
⑦硫酸钡在熔融状态能够导完全电离产生钡离子和硫酸根离子而导电的化合物,是强电解质,不导电;
⑧酒精在水溶液和熔融状态下都不能导电的化合物,是非电解质,不导电;
⑨熔化的KNO3完全电离产生自由移动钾离子和硝酸根离子,属于强电解质,含有自由移动的离子,能够导电;
⑩铁是单质,既不是电解质,也不是非电解质,含有自由电子,能够导电;
所以:(1)以上物质能导电的是①③⑨⑩;
故答案为:①③⑨⑩;
(2)以上物质属于强电解质的是:④⑦⑨;
故答案为:④⑦⑨;
(3)以上物质属于弱电解质的是:⑥;
故答案为:⑥;
(4)以上物质属于非电解质的是:②⑤⑧;
故答案为:②⑤⑧.
点评 本题考查了电解质与非电解质、强电解质与弱电解质的概念,注意掌握强弱电解质、电解质与非电解质的概念及判断方法是解题关键,题目难度不大.

练习册系列答案
 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目
13.飞船内安装盛有Na2O2的装置,它的用途是产生氧气.下列关于Na2O2的叙述正确的是( )
| A. | Na2O2中阴、阳离子的个数比为1:1 | |
| B. | Na2O2分别与水及CO2反应产生相同量的O2时,需要水和CO2的质量相等 | |
| C. | Na2O2分别与水及CO2反应产生相同量的O2时,转移电子的物质的量相等 | |
| D. | Na2O2的漂白原理与SO2的漂白原理相同 |
14.COCl2的分解反应为COCl2(g)═Cl2(g)+CO(g)△H=+108kJ•mol-1.反应体系平衡后,各物质的浓度在不同条件下的变化状况如下图所示(第10min到14min的COCl2浓度变化曲线未示出):比较反应物COCl2在5-6min和15-16min时平均反应速率的大小:v(5-6)_v(15-16)( )
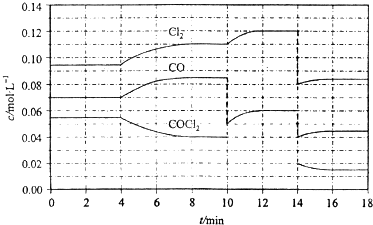

| A. | < | B. | = | ||
| C. | > | D. | 条件不足,无法判断 |
11.设NA 表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,0.1 mol Cl2 溶于水,转移的电子数目为0.2NA | |
| B. | 标准状况下,33.6L SO3中含有硫原子的数目为1.5NA | |
| C. | 50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA | |
| D. | 某密闭容器盛有0.1molN2和0.3molH2,在一定条件下充分反应,转移电子的数目小于0.6NA |
8.一定条件下,4mol A气体和2mol B气体在2L的密闭容器中发生反应:2A(g)+B(g)?3C(g),经2s后测得C的浓度为0.9mol•L-1,下列说法正确的是( )
| A. | 2s末A和B的转化率相同 | |
| B. | 2s末A的浓度为0.6mol/L | |
| C. | 反应速率$\frac{{v}_{(A)}}{{v}_{(B)}}$=$\frac{1}{2}$ | |
| D. | 用B表示的平均反应速率为0.3mol/(L•s) |

 .
.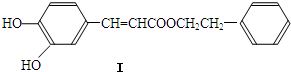
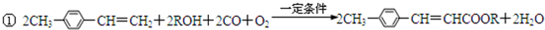
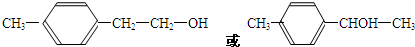 (写1种);由IV生成II的反应条件为NaOH醇溶液,加热.
(写1种);由IV生成II的反应条件为NaOH醇溶液,加热.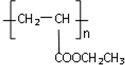 可用于制备涂料,其单体结构简式为CH2=CHCOOCH2CH3.利用类似反应①的方法,仅以乙烯为有机物原料合成该单体,涉及的反应方程式为(提示:共有两步反应方程式)CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH,2CH2=CH2+2CH3CH2OH+2CO+O2$\stackrel{催化剂}{→}$2CH2=CHCOOCH2CH3+2H2O.
可用于制备涂料,其单体结构简式为CH2=CHCOOCH2CH3.利用类似反应①的方法,仅以乙烯为有机物原料合成该单体,涉及的反应方程式为(提示:共有两步反应方程式)CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH,2CH2=CH2+2CH3CH2OH+2CO+O2$\stackrel{催化剂}{→}$2CH2=CHCOOCH2CH3+2H2O.