题目内容
17.同温同压下两个容积相等的贮气瓶,一个装有CO,一个装有N2和C2H4的混合气体,两瓶气体一定不相同的是( )| A. | 分子总数 | B. | 总质量 | C. | 原子总数 | D. | 密度 |
分析 同温同压下两个容积相等的贮气瓶,一个装有CO,一个装有N2和C2H4的混合气体,则CO与N2、C2H4的总物质的量相等,则含有分子数目相等,各物质的摩尔质量均为28g/mol,则质量相等、密度相等,乙烯分子含有6个原子,而CO、N2为双原子分子,则含有原子数目一定不相等.
解答 解:同温同压下两个容积相等的贮气瓶,一个装有CO,一个装有N2和C2H4的混合气体,则CO与N2、C2H4的总物质的量相等,
A.两瓶容器为气体的物质的量相等,则含有分子总数相等,故A不选;
B.两瓶容器为气体的物质的量相等,各物质的摩尔质量均为28g/mol,气体则质量相等,故B不选;
C.乙烯分子含有6个原子,而CO、N2为双原子分子,则含有原子数目一定不相等,故C选;
D.气体总质量相等,气体体积相等,则密度相等,故D不选,
故选:C.
点评 本题考查阿伏伽德罗定律及推论,难度不大,有利于基础知识的巩固.

练习册系列答案
相关题目
8.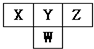 如图是周期表中短周期的一部分.已知Y和W原子能形成两种造成酸雨的有害气体,则下列说法中不正确的是( )
如图是周期表中短周期的一部分.已知Y和W原子能形成两种造成酸雨的有害气体,则下列说法中不正确的是( )
 如图是周期表中短周期的一部分.已知Y和W原子能形成两种造成酸雨的有害气体,则下列说法中不正确的是( )
如图是周期表中短周期的一部分.已知Y和W原子能形成两种造成酸雨的有害气体,则下列说法中不正确的是( )| A. | 原子半径的大小顺序是W>Y>Z | |
| B. | X的氢化物没有Z的氢化物稳定 | |
| C. | Z元素的最高价氧化物的水化物的酸性最强 | |
| D. | Y的氢化物比W的氢化物沸点高,是因为分子间存在氢键 |
5. 炼铁的还原剂CO是由焦炭和CO2反应而得,现将焦炭与CO2放入体积为2L的密闭容
炼铁的还原剂CO是由焦炭和CO2反应而得,现将焦炭与CO2放入体积为2L的密闭容
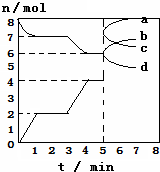
器中,高温下进行下列反应:C(s)+CO2(g)?2CO(g)△H=QkJ/mol,如图为CO2、CO的物质的量n随时间t的变化关系图,下列说法正确的( )
 炼铁的还原剂CO是由焦炭和CO2反应而得,现将焦炭与CO2放入体积为2L的密闭容
炼铁的还原剂CO是由焦炭和CO2反应而得,现将焦炭与CO2放入体积为2L的密闭容器中,高温下进行下列反应:C(s)+CO2(g)?2CO(g)△H=QkJ/mol,如图为CO2、CO的物质的量n随时间t的变化关系图,下列说法正确的( )
| A. | 3min时温度由T1升高到T2,则Q>0,重新平衡时K(T2):K(T1)=14﹕3 | |
| B. | 当容器内的压强不变时,该反应一定达到平衡状态,且$\frac{P(平衡)}{P(开始)}$<1 | |
| C. | 0~1min,v(CO)=1mol/(L•min);1~5min时,v正(CO)=v逆(CO2) | |
| D. | 5min时再充入一定量的CO,a、d曲线分别表示n(CO)、n(CO2)的变化 |
12.下列离子检验正确的是( )
| A. | 加入硝酸银溶液时有白色沉淀,说明溶液中含有Cl- | |
| B. | 加入BaCl2产生白色沉淀,加入稀盐酸不溶解,说明溶液中含有SO42- | |
| C. | 加入NaOH溶液,加热产生无色刺激性能使湿润的红色石蕊试纸变蓝的气体,说明溶液中一定含有NH4+ | |
| D. | 加入氢氧化钡溶液时,有白色沉淀生成,再加稀盐酸时,白色沉淀溶解,产生可使澄清石灰水变浑浊的无色无味气体,则溶液中一定含有CO32- |
2.把下列物质的水溶液蒸干、灼烧后,得到的固体为原先溶质的是( )
| A. | Na2CO3 | B. | AlCl3 | C. | Na2SO3 | D. | NH4HCO3 |
7.下列说法不正确的是( )
| A. | 检验Cl-离子的试剂是硝酸银和硝酸 | |
| B. | 配制一定物质的量浓度溶液时,未洗涤烧杯和玻璃棒,结果会偏低 | |
| C. | 配制一定物质的量浓度溶液时,容量瓶中有少量蒸馏水,对浓度无影响 | |
| D. | 向溶液中加入BaCl2溶液后生成白色沉淀,即可证明有SO${\;}_{4}^{2-}$ |


 根据原子结构、元素周期表和元素周期律的知识回答下列问题:
根据原子结构、元素周期表和元素周期律的知识回答下列问题: .
.