��Ŀ����
�±���Ԫ�����ڱ���һ����, ��Ա��еĢ١�����Ԫ��,��д���пհ�(��д��Ų��÷�)��
��1������ЩԪ����,��ѧ��������õ��ǣ� ������Ԫ�ط��ţ�
��2��������������ˮ�����У�������ǿ�Ļ�����Ļ�ѧʽ�� ��������ǿ�Ļ�����Ļ�ѧʽ�ǣ� ��
��3���ȽϢ���ݵ�����������Ӧ��ˮ��� ������ǿ���ѧʽ������ͨ�� ˵����д��Ӧ�Ļ�ѧ����ʽ����
��4��ʵ������ȡ�ڵ��⻯��Ļ�ѧ����ʽ ��
�ڵ��⻯����ڵ�����������ˮ���ﷴӦ���õIJ��ﻯѧʽΪ ��
��5���ڿ����γɶ������������һ���Ǻ���ɫ���壬���÷���ʽ˵�������岻�˲�����ˮ���ռ���ԭ�� ���û�ѧ����ʽ��ʾ����
��6���ȽϢ�����⻯� ���ȶ����ѧʽ����
��7��д���ܵĵ�����ˮ��Ӧ�����ӷ���ʽ ��
��8��д����Ԫ�ص����ӽṹʾ��ͼ ,�����Ӱ뾶 S2-�������������д����Ԫ�������ڱ���λ�� ��
| �� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0�� |
| 2 | | | | �� | �� | �� | | |
| 3 | �� | | | �� | | �� | �� | �� |
| 4 | �� | | | | | | �� | |
��1������ЩԪ����,��ѧ��������õ��ǣ� ������Ԫ�ط��ţ�
��2��������������ˮ�����У�������ǿ�Ļ�����Ļ�ѧʽ�� ��������ǿ�Ļ�����Ļ�ѧʽ�ǣ� ��
��3���ȽϢ���ݵ�����������Ӧ��ˮ��� ������ǿ���ѧʽ������ͨ�� ˵����д��Ӧ�Ļ�ѧ����ʽ����
��4��ʵ������ȡ�ڵ��⻯��Ļ�ѧ����ʽ ��
�ڵ��⻯����ڵ�����������ˮ���ﷴӦ���õIJ��ﻯѧʽΪ ��
��5���ڿ����γɶ������������һ���Ǻ���ɫ���壬���÷���ʽ˵�������岻�˲�����ˮ���ռ���ԭ�� ���û�ѧ����ʽ��ʾ����
��6���ȽϢ�����⻯� ���ȶ����ѧʽ����
��7��д���ܵĵ�����ˮ��Ӧ�����ӷ���ʽ ��
��8��д����Ԫ�ص����ӽṹʾ��ͼ ,�����Ӱ뾶 S2-�������������д����Ԫ�������ڱ���λ�� ��
��1��Ar��
��2��HClO4 KOH��
��3��H2CO3 Na2SiO3+CO2+H2O=Na2CO3+H2SiO3��
��4��2NH3Cl+Ca(OH)2 CaCl2+2NH3��+2H2O NH4NO3��
CaCl2+2NH3��+2H2O NH4NO3��
��5��3NO2+H2O=2HNO3+NO
��6��H2O
��7��2Na+2H2O=2Na++2OH-+H2��
��8��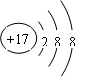 ��<���������ڢ�A��
��<���������ڢ�A��
��2��HClO4 KOH��
��3��H2CO3 Na2SiO3+CO2+H2O=Na2CO3+H2SiO3��
��4��2NH3Cl+Ca(OH)2
 CaCl2+2NH3��+2H2O NH4NO3��
CaCl2+2NH3��+2H2O NH4NO3����5��3NO2+H2O=2HNO3+NO
��6��H2O
��7��2Na+2H2O=2Na++2OH-+H2��
��8��
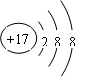 ��<���������ڢ�A��
��<���������ڢ�A������������⼸��Ԫ�طֱ��ǣ���C����N ����O����Na����Si����S ����Cl ; ��Ar; ��K; ��Br��ͬһ���ڵ�Ԫ�أ�����ԭ������������Ԫ�صĽ������������ǽ���������ǿ�����������õĶ�������Ԫ�ؽ�������ͬһ�����Ԫ�أ����ϵ��£�Ԫ�ص�ԭ�Ӱ뾶������Ԫ�صĽ���������ǿ���ǽ�������������1������ЩԪ����,��ѧ��������õ��Ǣ�ArԪ�أ� ��2��������������ˮ�����У�������ǿ�Ļ������HClO4��������ǿ�Ļ�����KOH����3��C��Si��ͬһ�����Ԫ�أ��ǽ�����C>Si��Ԫ�صķǽ�����Խǿ��������������Ӧ��ˮ��������Ծ�Խǿ����˱ȽϢ���ݵ�����������Ӧ��ˮ���������ǿ����H2CO3������ͨ����ӦCO2+H2O + Na2SiO3= H2SiO3��+ Na2CO3֤������4����ʵ����һ�����������������ȡ�����ġ���ȡNH3�ķ���ʽΪ2NH3Cl+Ca(OH)2
 CaCl2+2NH3��+2H2O���ڵ��⻯��NH3��ڵ�����������ˮ����HNO3��Ӧ��NH3+ HNO3= NH4NO3.��˷�Ӧ������NH4NO3����5��NO2�Ǻ���ɫ���壬�����ܽ���ˮ��������Ӧ3NO2+H2O=2HNO3+NO����6����O���S��ͬһ�����Ԫ�أ����ڷǽ�����O>S��Ԫ�صķǽ�����Խǿ�����Ӧ���⻯����ȶ��Ծ�Խǿ��Ԫ���ȶ���H2O >H2S����7��Na��ˮ��Ӧ�����ӷ���ʽΪ��2Na+2H2O=2Na++2OH-+H2������8��Cl-���ӽṹʾ��ͼΪ��
CaCl2+2NH3��+2H2O���ڵ��⻯��NH3��ڵ�����������ˮ����HNO3��Ӧ��NH3+ HNO3= NH4NO3.��˷�Ӧ������NH4NO3����5��NO2�Ǻ���ɫ���壬�����ܽ���ˮ��������Ӧ3NO2+H2O=2HNO3+NO����6����O���S��ͬһ�����Ԫ�أ����ڷǽ�����O>S��Ԫ�صķǽ�����Խǿ�����Ӧ���⻯����ȶ��Ծ�Խǿ��Ԫ���ȶ���H2O >H2S����7��Na��ˮ��Ӧ�����ӷ���ʽΪ��2Na+2H2O=2Na++2OH-+H2������8��Cl-���ӽṹʾ��ͼΪ��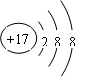 ��Cl-��S2-��������Ų�����2��8��8.���Ӳ�ṹ��ͬ�����ڵ��Ӳ�ṹ��ͬ������˵�����ӵĺ˵����Ҳ�࣬���Ӱ뾶��ԽС��������Ӱ뾶Cl-<S2-����Ԫ��Br�����ڱ���λ����λ�ڵ������ڵڢ�A�塣
��Cl-��S2-��������Ų�����2��8��8.���Ӳ�ṹ��ͬ�����ڵ��Ӳ�ṹ��ͬ������˵�����ӵĺ˵����Ҳ�࣬���Ӱ뾶��ԽС��������Ӱ뾶Cl-<S2-����Ԫ��Br�����ڱ���λ����λ�ڵ������ڵڢ�A�塣
��ϰ��ϵ�д�
 ��ս�п�����ϵ�д�
��ս�п�����ϵ�д�
�����Ŀ