题目内容
A元素的最高价离子0.5 mol被还原成中性原子时,要得到6.02×1023个电子。它的单质同盐酸充分反应时,放出0.02 g H2,用去0.4 g A。B元素的原子核外电子层数与A相同,且B元素形成的单质是红棕色液体。
(1)写出这两种元素的名称:A ,B 。
(2)用结构示意图表示A、B两元素常见离子:A ,B 。
(3)用电子式表示A、B形成的化合物。
(1)写出这两种元素的名称:A ,B 。
(2)用结构示意图表示A、B两元素常见离子:A ,B 。
(3)用电子式表示A、B形成的化合物。
(1)钙 溴
(2)Ca2+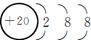 Br-
Br-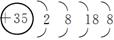
(3)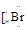 ∶]-Ca2+
∶]-Ca2+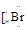 ∶]-
∶]-
(2)Ca2+
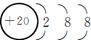 Br-
Br-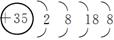
(3)
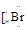 ∶]-Ca2+
∶]-Ca2+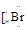 ∶]-
∶]-从B的单质为红棕色液体可推知B的单质为Br2。溴原子有4个电子层,所以A原子也有4个电子层,由0.5 mol A元素的最高价离子被还原成原子时能得到电子1 mol,说明A的离子为+2价,即A原子最外层有2个电子。
依题意:A ~ H2
M 2
0.4 g 0.02 g
M=40 则A为钙元素。
依题意:A ~ H2
M 2
0.4 g 0.02 g
M=40 则A为钙元素。

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目

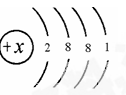
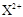 的核外电子数目为18,则X在第四周期第ⅡA族
的核外电子数目为18,则X在第四周期第ⅡA族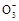 所含电子数比硝酸根离子N
所含电子数比硝酸根离子N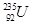 和
和 是中子数不同质子数相同的同种核素
是中子数不同质子数相同的同种核素