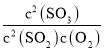题目内容
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.无色澄清的溶液:Na+、NH![]() 、S2-、ClO-
、S2-、ClO-
B.能使石蕊变红的溶液:Fe2+、Na+、NO![]() 、SO
、SO![]()
C.水电离的c(H+)=1×10-13mol·L-1的溶液中:Ba2+、K+、HCO![]() 、S2-
、S2-
D.![]() =10-12的溶液中:Na+、NO
=10-12的溶液中:Na+、NO![]() 、AlO
、AlO![]() 、CO
、CO![]()
【答案】D
【解析】
A.次氯酸根具有氧化性,会将S2-氧化,不能大量共存,故A不符合题意;
B.使石蕊变红的溶液显酸性,酸性溶液中硝酸根会将亚铁离子氧化,故B不符合题意;
C.水电离的c(H+)=1×10-13mol·L-1的溶液中水的电离受到抑制,既可能显碱性也可能显酸性,酸性和碱性溶液中,碳酸氢根都不能大量存在,酸性溶液中硫离子不能大量存在,故C不符合题意;
D.![]() =10-12的溶液显碱性,碱性溶液中四种离子相互不反应,也不与氢氧根反应,所以可以大量共存,故D符合题意;
=10-12的溶液显碱性,碱性溶液中四种离子相互不反应,也不与氢氧根反应,所以可以大量共存,故D符合题意;
故答案为D。

 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案【题目】CO2是一种廉价的碳资源,其综合利用具有重要意义。
(一)CO2的化学捕获:
(1)CO2可以被NaOH溶液捕获。若所得溶液pH=13,CO2主要转化为___(写含碳粒子符号)。(室温下,H2CO3的Ka1=4.3×10﹣7;Ka2=5.6×10﹣11)
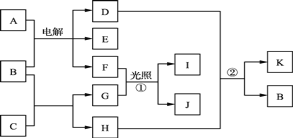
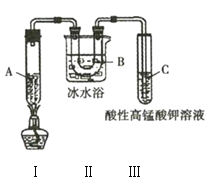
(2)固体氧化物电解池(SOEC)用于高温共电解CO/H2,既可实现CO2的减排又可高效制备合成气(CO/H2),其工作原理如图。写出电极A发生的电极反应式___。

(二)CO2的综合利用
(1)CO2与CH4经催化重整制得合成气:
反应Ⅰ.CH4(g)H+CO2(g)2CO(g)+2H2(g)△H1
已知氢气、一氧化碳和甲烷的标准燃烧热(25℃)如表所示
物质 | H2(g) | CO(g) | CH4(g) |
标准燃烧热△H/kJmol﹣1 | ﹣285.8 | ﹣283.0 | ﹣890.3 |
则反应I的△H=___kJmol﹣1。
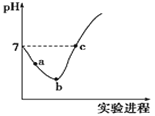
(2)用CO2催化加氢制取二甲醚的反应为:反应Ⅱ.2CO2(g)+6H2(g)CH3OCH3(g)+3H2O(g),在10L恒容密闭容器中,均充入2mol CO2和6moH2,分别以铱(Ir)和铈(Ce)作催化剂,反应进行相同的时间后测得的CO2的转化率α(CO2)随反应温度的变化情况如图1。
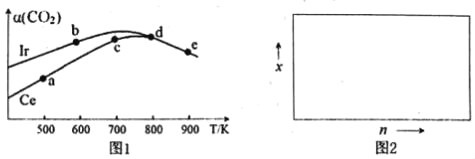
①根据图1,下列说法不正确的是___。
A.反应Ⅱ的△H<0,△S<0
B.用Ir和Ce作催化剂时,反应Ⅱ的活化能更低的是Ce
C.状态d时,v(正)<v(逆)
D.从状态b到d,α(CO2)先增大后减小,减小的原因可能是温度升高平衡逆向移动
②状态e(900K)时,α(CO2)=50%,则此时的平衡常数K=___。
③若H2和CO2的物质的量之比为n:1,900K时相应平衡体系中二甲醚的物质的量分数为x,请在图2中绘制x随n变化的示意图。_______