题目内容
【题目】X是一种新型无机非金属材料,具有耐磨、耐腐蚀、抗冷热冲击性。有关生产过程如下:
![]()
为了确定C的组成,某同学进行了以下的探究过程。已知F、G都是难溶于水和稀硝酸的白色沉淀,I可作光导纤维。
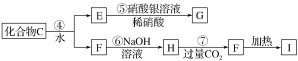
按要求回答下列问题:
(1)C的化学式为________;X的化学式为________。
(2)写出下列方程式:
反应②的化学方程式_________________________________________________;
反应⑦的离子方程式_____________________________________________________。
【答案】SiCl4 Si3N4 SiCl4+4NH3=Si(NH2)4+4HCl SiO32-+2H2O+2CO2=H2SiO3↓+2HCO3-
【解析】
由I可作光导纤维知,I为SiO2,根据题给第二个框图中的转化关系和“F、G都是难溶于水和稀硝酸的白色沉淀”知F为硅酸,H为硅酸钠;由E→G是加入了硝酸银和稀硝酸,生成了难溶于水和稀硝酸的白色沉淀,则E中含有氯离子;则化合物C中含硅、氯两种元素,故C为SiCl4,D为Si(NH2)4,X为Si3N4。
I可做光导纤维,所以I是二氧化硅,则F是硅酸,H是硅酸钠。又因为F、G都是难溶于水和稀硝酸的白色沉淀,所以G是氯化银,因此C是SiCl4,则A是硅,B是氯气。根据X的性质可知,X是原子晶体,所以X是Si3N4。由转化关系可知,SiCl4与NH3反应生成Si(NH2)4,根据原子守恒可知还生成HCl,由于氨气过量,故应生成NH4Cl;CO2是过量的,因此生成物是碳酸氢钠与硅酸。
(1)由以上分析可知C为SiCl4,具有甲烷的结构,为正四面体,X为Si3N4;
(2)由转化关系可知,SiCl4与NH3反应生成Si(NH2)4,根据原子守恒可知还生成HCl,由于氨气过量,应生成NH4Cl,故反应于的反应方程式为:SiCl4+8NH3=Si(NH2)4+4NH4Cl;
(3)CO2是过量的,因此生成物是碳酸氢钠与硅酸,反应舆的离子方程式为:SiO32-+2H2O+2CO2=2H2SiO3↓+2HCO3-。

【题目】研究生铁的锈蚀,下列分析不正确的是
序号 | ① | ② | ③ |
实验 |
|
|
|
现象 | 8小时未观察 到明显锈蚀 | 8小时未观察 到明显锈蚀 | 1小时观察 到明显锈蚀 |
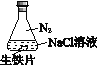
A. ①中,NaCl溶液中溶解的O2不足以使生铁片明显锈蚀
B. ②中,生铁片未明显锈蚀的原因之一是缺少H2O
C. ③中正极反应:O2+4e+ 2H2O ==4OH
D. 对比①②③,说明苯能隔绝O2