题目内容
已知在一定条件下,2SO2(g)+O2(g) 2SO3(g) ΔH="-Q" kJ·mol-1。向一密闭容器中加入2 mol SO2和1 mol O2,达平衡时SO2的转化率为90%,放出的热量为Q1 kJ;向另一相同容器中加入2 mol SO3,在相同条件下,达平衡时吸收的热量为Q2 kJ,则下列关系中正确的是( )
2SO3(g) ΔH="-Q" kJ·mol-1。向一密闭容器中加入2 mol SO2和1 mol O2,达平衡时SO2的转化率为90%,放出的热量为Q1 kJ;向另一相同容器中加入2 mol SO3,在相同条件下,达平衡时吸收的热量为Q2 kJ,则下列关系中正确的是( )
| A.Q>Q1>Q2 | B.Q1>Q2>Q | C.Q1>Q>Q2 | D.Q1=Q2>Q |
A
解析

某些化学键键能数据如下:
| 化学键 | H—H | Cl—Cl | H—Cl |
| 键能/ kJ·mol-1 | 436 | 243 | 431 |
则下列热化学方程式不正确的是 ( )
A.
 H2(g)+
H2(g)+ Cl2(g)=HCl(g) ΔH=-91.5 kJ·mol-1
Cl2(g)=HCl(g) ΔH=-91.5 kJ·mol-1B.H2(g)+Cl2(g)=2HCl(g)ΔH=-183 kJ·mol-1
C.
 H2(g)+
H2(g)+ Cl2(g)=HCl(g)ΔH=+91.5 kJ·mol-1
Cl2(g)=HCl(g)ΔH=+91.5 kJ·mol-1D.2HCl(g)=H2(g)+Cl2(g)ΔH=+183 kJ·mol-1
已知反应:①101 kPa时,2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1
②稀溶液中,H+(aq)+OH-(aq)=H2O(l)ΔH=-57.3 kJ·mol-1
③H2(g) O2(g)=H2O(g)ΔH=-241.8 kJ·mol-1
O2(g)=H2O(g)ΔH=-241.8 kJ·mol-1
④H2O(g)=H2O(l)ΔH=-44.0 kJ·mol-1
下列结论正确的是( )
| A.碳的燃烧热大于110.5 kJ·mol-1 |
| B.浓硫酸与稀NaOH溶液反应生成1 mol水,放出57.3 kJ热量 |
| C.氢气的燃烧热为241.8 kJ·mol-1 |
| D.2H2(g)+O2(g)=2H2O(l)的反应热为ΔH=+571.6 kJ·mol-1 |
能源是当今社会发展的三大支柱之一。有专家提出:如果能够利用太阳能使燃料燃烧产物(如CO2、H2O、N2等)重新组合(如下图),可以节约燃料,缓解能源危机。在此构想的物质循环中太阳能最终转化为( )
| A.化学能 | B.热能 | C.生物能 | D.电能 |
已知:① 2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ·mol-1 ②H2(g)+S(g)=H2S(g) ΔH=-20.1 kJ·mol-1。
下列判断正确的是( )
| A.1 mol氢气完全燃烧生成液态水吸收热量241.8 kJ |
| B.1 mol H2O(g)和1 mol H2S(g)的能量相差221.7 kJ |
| C.由①②知,水的热稳定性小于硫化氢 |
| D.若反应②中改用固态硫,1 mol S(s)完全反应,放出的热量小于20.1 kJ |
已知:①2H2(g)+O2(g) 2H2O(g)ΔH="-483.6" kJ/mol
2H2O(g)ΔH="-483.6" kJ/mol
②H2(g)+S(g)=H2S(g) ΔH="-20.1" kJ/mol。下列判断正确的是( )
| A.1 mol氢气完全燃烧吸热241.8 kJ |
| B.1 mol H2O(g)和1 mol H2S(g)的能量相差221.7 kJ |
| C.由①②知,水的热稳定性小于硫化氢 |
| D.若反应②中改用固态硫,1 mol S(s)完全反应,放出的热量小于20.1 kJ |
下列与化学反应能量变化相关的叙述正确的是 ( )。
| A.生成物总能量一定低于反应物总能量 |
| B.酒精可用作燃料,说明酒精燃烧是释放能量的反应 |
| C.干冰气化需要吸收大量的热,这个变化是吸热反应 |
| D.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH不同 |
工业生产硫酸过程中,SO2在接触室中被催化氧化为SO3,已知该反应为放热反应。现将2 mol SO2、1 mol O2充入一密闭容器充分反应后,放出热量98.3 kJ,此时测得SO2的转化率为50%。下列热化学方程式正确的是 ( )。
A.2SO3(g)  2SO2(g)+O2(g)ΔH=+196.6 kJ·mol-1 2SO2(g)+O2(g)ΔH=+196.6 kJ·mol-1 |
B.2SO2(g)+O2(g)  SO3(g)ΔH=-98.3 kJ·mol-1 SO3(g)ΔH=-98.3 kJ·mol-1 |
C.SO2(g)+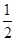 O2(g) O2(g) SO3(g)ΔH=+98.3 kJ·mol-1 SO3(g)ΔH=+98.3 kJ·mol-1 |
D.SO2(g)+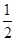 O2(g) O2(g) SO3(g)ΔH=-196.6 kJ·mol-1 SO3(g)ΔH=-196.6 kJ·mol-1 |
已知:①H2O(g)=H2O(l) ΔH1=-Q1 kJ·mol-1
②C2H5OH(g)=C2H5OH(l) ΔH2=-Q2 kJ·mol-1
③C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g) ΔH3=-Q3 kJ·mol-1
若使23 g液态无水酒精完全燃烧,最后恢复到室温,则放出的热量为(单位:kJ)( )
| A.Q1+Q2+Q3 |
| B.1.5Q1-0.5Q2+0.5Q3 |
| C.0.5Q1-1.5Q2+0.5Q3 |
| D.0.5(Q1+Q2+Q3) |