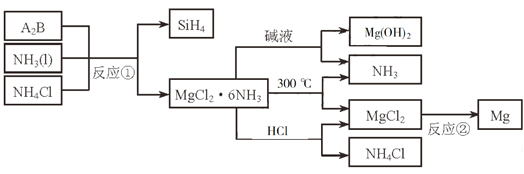
题目内容
【题目】C60具有完美的球形结构。之后Si60、N60等球形分子被不断制备出来。回答下列问题:
(1)Si的核外电子排布式为_______,C和N元素中第一电离能较大的是_______。
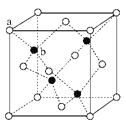
(2)富勒烯衍生物具有良好的光电性能,富勒烯(C60)的结构如右图所示,C60属于___晶体;C60分子中五元环与六元环的数目比为_____。

(已知简单多面体的顶点数V、棱数E及面数F间有如下关系:V-E+F=2)。
(3)N60的晶体中存在的作用力有_____(填字母标号)
A.共价键 B.离子键 C.氢键
D.范德华力 E.配位键 F.金属键
(4)立方氮化硼(BN)可做磨料,其结构与金刚石相似,二者具有相似性结构的原因是_______。
(5)金属M(相对原子质量为m)与N60形成的化合物晶体结构如右图所示(其中白球代表N60,黑球代表金属M),若其晶胞边长为k pm,NA代表阿伏加德罗常数的值,则其密度为______g·cm-3,该化合物中N60的配位数为______。
【答案】 1s22s22p63s23p2或[Ar]3s23p2 N 分子 3:5 AD 硼原子核外有3个价电子,氮原子核外有5个价电子。在立方氮化硼晶体中,每个硼原子除了利用3个价电子形成普通的共价键外,还可以提供空轨道,接受氮原子的孤对电子,形成一个配位键,于是在立方氮化硼晶体中硼原子和氨原子都采取sp3杂化方式,这和金刚石中C原子的轨道杂化方式一样,就形成了与金刚石类似的正四面体空间网络结构。  4
4
【解析】(1)Si是第14号元素,其核外电子排布式为1s22s22p63s23p2或[Ar]3s23p2,元素C、N属于同一周期元素且原子序数依次增大,同一周期元素的第一电离能随着原子序数的增大而增大,但第ⅤA族的大于第ⅥA族的,所以其第一电离能较大的是是N;(2)C60属于分子晶体;已知简单多面体的顶点数V、棱数E及面数F间有如下关系:V-E+F=2,富勒烯是C60,顶点为60,边数:每个碳原子分出来了三个键(不考虑双键),而碳原子是两两相连,所以一个碳原子占有1.5个键,也就是边数是顶点数的1.5倍, 90个,所以总共就有32个面,然后设五边形x个,六边形y个:x+y=32,每个五边形与五个六边形相邻,每个六边形与三个五边形和三个六边形相邻,所以5x=3y,两个式子解出x=12,y=20,故C60分子中五元环与六元环的数目比为12:20=3:5;(3)N60是分子晶体,存在的作用力有共价键、范德华力,答案选AD;(4)硼原子核外有3个价电子,氮原子核外有5个价电子。在立方氮化硼晶体中,每个硼原子除了利用3个价电子形成普通的共价键外,还可以提供空轨道,接受氮原子的孤对电子,形成一个配位键,于是在立方氮化硼晶体中硼原子和氨原子都采取sp3杂化方式,这和金刚石中C原子的轨道杂化方式一样,就形成了与金刚石类似的正四面体空间网络结构;(5)根据均摊法可得,一个晶胞中M的个数为4个,N60的个数为8![]() +6
+6![]() =4,一个晶胞的质量为
=4,一个晶胞的质量为![]() ,晶胞边长为k pm,则晶胞的体积为(k pm)3=k3
,晶胞边长为k pm,则晶胞的体积为(k pm)3=k3![]() ,故密度为
,故密度为 ;该化合物中N60的配位数为4。
;该化合物中N60的配位数为4。

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案【题目】亚硝酰氯(ClNO)是有机合成中常用的试剂。
巳知:①2NO2(g)+NaCl(s)![]() NaNO3(s)+ClNO(g)△H1=akJ·mol-1
NaNO3(s)+ClNO(g)△H1=akJ·mol-1
②4NO2(8)+2NaCl(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g)△H2=bkJ·mol-1
2NaNO3(s)+2NO(g)+Cl2(g)△H2=bkJ·mol-1
③2NO(g)+Cl2(g)![]() 2ClNO(g)△H3=ckJ·mol-1
2ClNO(g)△H3=ckJ·mol-1
(1)上述反应中,a、b、c之间满足的关系为_____________________。
(2)某温度下,在密闭容器中发生反应:2NO(g)+Cl2(g)![]() 2ClNO(g),正反应速率表达式为v正=k·cn(NO)·cm(Cl2)(k是反应速率常数,只与温度有关;n、m为反应级数,只取正数)。测得正反应速率与浓度的关系如下表所示:
2ClNO(g),正反应速率表达式为v正=k·cn(NO)·cm(Cl2)(k是反应速率常数,只与温度有关;n、m为反应级数,只取正数)。测得正反应速率与浓度的关系如下表所示:
序号 | c(NO)/mol·L-1 | c(Cl2)/mol·L-1 | v正/mol·L-1·min-1 |
ⅰ | 0.100 | 0.100 | 0.144 |
ⅱ | 0.100 | 0.200 | 0.288 |
ⅲ | 0.200 | 0.100 | 0.576 |
①n=_____________,m=_____________。
②反应达到平衡后,其他条件不变时,缩小容器体积瞬间,v正_____________v逆(填“>"“<”或“=")。NO的平衡转化率_____________(填“增大”“减小”或“不变”)。
(3)在2L恒容密闭容器中充入0.8molClNO(g),发生反应:2ClNO(g)![]() Cl2(g)+2NO(g) △H,测得c(Cl2)与温度和时间的关系如图1所示。300℃时达到平衡后,温度与平衡常数负对数(-lgK)的关系如图2所示。
Cl2(g)+2NO(g) △H,测得c(Cl2)与温度和时间的关系如图1所示。300℃时达到平衡后,温度与平衡常数负对数(-lgK)的关系如图2所示。
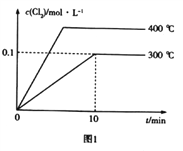

①a=_____________。
②图2中符合题意的曲线为_____________(填“Ⅰ”或“Ⅱ”)。