题目内容
【题目】对以下两个反应的分析说法正确的是
2Al+2NaOH+2H2O=2NaAlO2 +3H2↑ 2Na2O2+2H2O=4NaOH+O2↑
A.铝与氢氧化钠溶液的反应中,铝是还原剂,H2O和NaOH都是氧化剂
B.铝与氢氧化钠溶液的反应中,当有3mol电子转移,就会生成3mol还原产物H2
C.在过氧化钠与水的反应中,氧化剂Na2O2,还原剂为H2O
D.在过氧化钠与水的反应中,每有1mol电子转移,就有0.5molO2生成
【答案】D
【解析】
A.铝与氢氧化钠溶液的反应中,铝是还原剂,水是氧化剂,A项错误;
B.根据方程式可以看出每生成3mol氢气,反应中要转移6mol电子,生成氢气数:转移电子数为1:2,因此B项错误;
C.过氧化钠中-1价的氧发生歧化反应,得到0价的氧气和-2价的![]() ,C项错误;
,C项错误;
D.根据方程式可以看出每生成1mol氧气,反应中要转移2mol电子,生成氧气数:转移电子数为1:2,D项正确;
答案选D。

 阅读快车系列答案
阅读快车系列答案【题目】Li4Ti5O12和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿(主要成分为FeTiO3,还含有少量MgO、SiO2等杂质)来制备,工艺流程如下:
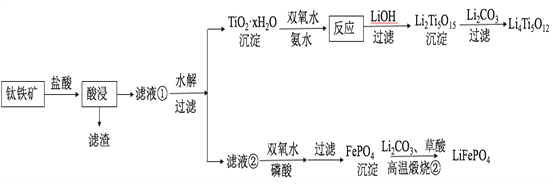
回答下列问题:
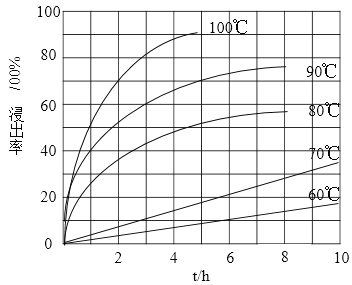
(1)“酸浸”实验中,铁的浸出率结果如下图所示。由图可知,当铁的净出率为70%时,所采用的实验条件为___________________。
(2)“酸浸”后,钛主要以TiOCl42-形式存在,写出相应反应的离子方程式__________________。
(3)TiO2·xH2O沉淀与双氧水、氨水反应40 min所得实验结果如下表所示:
温度/℃ | 30 | 35 | 40 | 45 | 50 |
TiO2·xH2O转化率% | 92 | 95 | 97 | 93 | 88 |
分析40℃时TiO2·xH2O转化率最高的原因__________________。
(4)Li2Ti5O15中Ti的化合价为+4,其中过氧键的数目为__________________。
(5)若“滤液②”中c(Mg2+)=0.02 mol/L,加入双氧水和磷酸(设溶液体积增加1倍),使Fe3+恰好沉淀完全即溶液中c(Fe3+)=1×10-5 mol/L,此时是否有Mg3(PO4)2沉淀生成?___________(列式计算)。
FePO4、Mg3(PO4)2的Ksp分别为1.3×10-22、1.0×10-24。
(6)写出“高温煅烧②”中由FePO4制备LiFePO4的化学方程式______。
【题目】(1)如图 1 是化学反应中物质变化和能量变化的示意图。在锌与稀盐酸的反应中,E1 _____ E2 (填“>”或“<”或“=”)
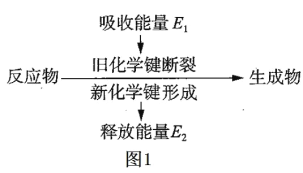
(2)工业上利用 CO 和 H2 在催化剂作用下合成甲醇:CO(g)+2H2(g) ![]() CH3OH(g) ,已知反应中有关物质的化学键键能数据如下表所示:
CH3OH(g) ,已知反应中有关物质的化学键键能数据如下表所示:
化学键 | H—H | C—O | C≡O | H—O | C—H |
E/(kJ/mol) | 436 | 343 | 1076 | 465 | 413 |
则 CO(g)+2H2(g) ![]() CH3OH(g) △H=_____kJmol-1
CH3OH(g) △H=_____kJmol-1
(3)化学兴趣小组进行测定中和热的实验,装置如图,步骤如下。
a.用量筒量取 50 mL 0.50 mol·L-1 盐酸倒入如图装置的小烧杯中,测出盐酸温度。 b.用另一量筒量取 50 mL 0.55 mol·L-1 NaOH 溶液,并用另一温度计测出其温度。 c.将 NaOH 溶液倒入小烧杯中,使之混合均匀,测得混合液最高温度。
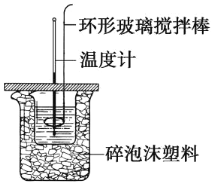
①实验中,倒入 NaOH 溶液的正确操作是_____。
A.一次性快速倒入 B.分 3 次倒入 C.边搅拌边慢慢倒入
②若将各含 1mol 溶质的 NaOH 稀溶液、Ca(OH)2 稀溶液、稀氨水,分别与足量的稀盐酸反应,放出的热量分别为 Q1、Q2、Q3,则 Q1、Q2、Q3 的关系为_____。
③假设盐酸和氢氧化钠溶液的密度都是 1 g·cm-3,又知中和反应后生成溶液的比热容c=4.18 J·g-1·℃-1。某学生实验后,处理数据,得到实验变化的温度为 3.20℃。该实验测得中和热ΔH =_____(结果保留一位小数)。