题目内容
【题目】海洋是生命的摇篮,海水不仅是宝贵的水资源,而且蕴藏着丰富的化学资源。
I.(1)海水中所得粗盐中通常含Ca2+、Mg2+、SO42-等杂质,为了得到精盐,下列试剂加入的先后顺序正确的是________
A.BaCl2→Na2CO3→NaOH→HCl B.NaOH→BaCl2→Na2CO3→HCl
C.BaCl2→NaOH→Na2CO3→HCl D. Na2CO3→NaOH→BaCl2→HCl
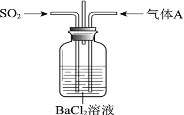
(2)为了检验精盐中是否含有SO42-,正确的方法是____________________________。
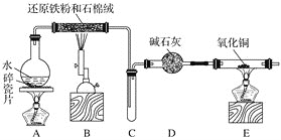
II.海藻中提取碘的流程如图所示
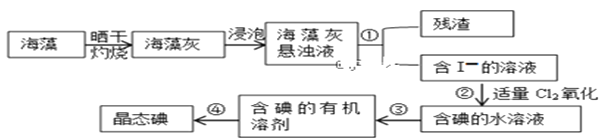
(3)灼烧过程中,需使用到的(除泥三角外)实验仪器有____________
A.试管 B.瓷坩埚 C.坩埚钳 D.蒸发皿 E.酒精灯 F.三脚架
(4)指出提取碘的过程中有关实验操作名称:①________③__________④_________
(5)步骤②反应的离子方程式为___________________,该过程氧化剂也可以用H2O2,将等物质的量的I-转化为I2,所需Cl2和H2O2的物质的量之比为__________
(6)下列关于海藻提取碘的说法,正确的是_________
A.含碘的有机溶剂呈现紫红色
B.操作③中先放出下层液体,然后再从下口放出上层液体
C.操作④时,温度计的水银球应伸入液面以下但不能触碰到蒸馏烧瓶的底部
【答案】ABC 取少量精盐溶于水,先加入稀盐酸,无现象,向其中加入氯化钡溶液,若产生沉淀,则含有硫酸根离子 BCEF 过滤 萃取分液 蒸馏 Cl2+2I-![]() 2Cl-+I2 1:1 A
2Cl-+I2 1:1 A
【解析】
I.海水中所得粗盐中通常含Ca2+、Mg2+、SO42-等杂质,为了得到精盐,Ca2+用碳酸钠转化为沉淀、Mg2+用NaOH转化为沉淀、SO42-用氯化钡溶液转化为沉淀,先除去Mg2+或SO42-,然后再加入过量的碳酸钠除去Ca2+以及过量的Ba2+杂质,过滤后再加盐酸除去过量的NaOH和碳酸钠;关键点:根据不能产生新杂质的要求排序,前面加入的过量溶液应用后加入的溶液除去;检验硫酸根离子一定要防止其他离子干扰;
II.将海藻晒干,放到坩埚中灼烧得到海藻灰,海藻灰悬浊液过滤除掉残渣,得到含碘离子的溶液,通入氯气将碘离子氧化为碘单质,加入有机试剂苯或四氯化碳将碘单质萃取到有机层,分液得有机溶液,再蒸馏得到晶态碘;
(3)固体灼烧用到的仪器有坩埚,坩埚钳,泥三角,三脚架,酒精灯;
(4)海藻灰悬浊液过滤除掉残渣,得到含碘离子的溶液,通入氯气将碘离子氧化为碘单质,加入有机试剂苯或四氯化碳将碘单质萃取到有机层,分液得有机溶液,再蒸馏得到晶态碘;
(5)选择氧化剂将碘离子氧化为碘单质,根据得失电子数相等计算;
(6)A.碘单质在有机溶剂中呈现紫红色;
B.没有确定萃取剂是谁,没有办法确定有机溶液在上层还是下层;
C.温度计的水银球应该在蒸馏烧瓶支管口附近测量蒸气的温度;
I.(1)根据不能产生新杂质的要求排序,前面加入的过量溶液应用后加入的溶液除去的原则确定除杂顺序,所以碳酸钠必须在氯化钡后面,过滤后再加盐酸除去过量的NaOH和碳酸钠,选项A、B、C满足;
正确答案:ABC。
(2)检验硫酸根离子,应该先加入盐酸无现象,排除其他杂志离子的干扰,再加入氯化钡产生白色沉淀;
正确答案:少量精盐溶于水,先加入稀盐酸,无现象,向其中加入氯化钡溶液,若产生沉淀,则含有硫酸根离子。
II. 现将海藻晒干,放到坩埚中灼烧得到海带灰,海藻灰悬浊液过滤除掉残渣,得到含碘离子的溶液,通入氯气将碘离子氧化为碘单质,加入有机试剂苯或四氯化碳将碘单质萃取到有机层,分液得有机溶液,再蒸馏得到晶态碘;
(3)固体灼烧用到的仪器有坩埚,坩埚钳,泥三角,三脚架,酒精灯;
正确答案:BCEF。
(4)海藻灰悬浊液过滤除掉残渣,得到含碘离子的溶液,通入氯气将碘离子氧化为碘单质,加入有机试剂苯或四氯化碳将碘单质萃取到有机层,分液得有机溶液,再蒸馏得到晶态碘;
正确答案:过滤 萃取分液 蒸馏。
(5)Cl2+2I =2Cl-+I2,2I-+H2O2+2H+=I2+2H2O,将等物质的量的I-转化为I2,所需Cl2和H2O2的物质的量之比1:1;
正确答案:Cl2+2I =2Cl-+I2 1:1。
(6)A.碘单质在有机溶剂中呈现紫红色,故A正确;
B.没有确定萃取剂是谁,没有办法确定有机溶液在上层还是下层,故B不正确;
C.温度计的水银球应该在蒸馏烧瓶支管口附近测量蒸气的温度,故C不正确;
正确答案:A。

【题目】毒重石的主要成分为BaCO3(含Ca2+、Mg2+、Fe3+等杂质)。实验室利用毒重石制备BaCl2·2H2O的流程如下:
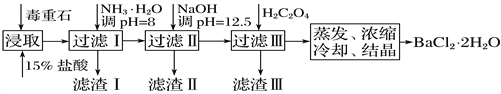
(1)毒重石用盐酸浸取前需充分研磨,目的是_________________________。
(2)已知:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9
Ca2+ | Mg2+ | Fe3+ | |
开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
完全沉淀时的pH | 13.9 | 11.1 | 3.2 |
加入NH3·H2O调pH=8可除去________(填离子符号),滤渣Ⅱ中含__________(填化学式)。加入H2C2O4时应避免过量,原因是______________________________。
(3)利用间接酸碱滴定法可测定Ba2+的含量,实验分两步进行。
已知:2CrO42-+2H+=Cr2O72-+H2O;Ba2++CrO42-=BaCrO4↓
步骤Ⅰ:移取x mL一定浓度的Na2CrO4溶液于锥形瓶中,加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V0 mL。
步骤Ⅱ:移取y mL BaCl2溶液于锥形瓶中,加入x mL与步骤Ⅰ相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1 mL。
滴加盐酸标准液时应使用酸式滴定管,“0”刻度位于滴定管的________(填“上方”或“下方”)。BaCl2溶液的浓度为_______mol·L-1。若步骤Ⅱ中滴加盐酸时有少量待测液溅出,Ba2+浓度测量值将________(填“偏大”或“偏小”)。