题目内容
某同学用标准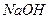 溶液来测定未知浓度的盐酸的浓度:
溶液来测定未知浓度的盐酸的浓度:
(1)配制250mL 0.5mol/L的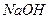 溶液所需的玻璃仪器为 。
溶液所需的玻璃仪器为 。
(2)用滴定管准确量取20.00mL未知浓度的盐酸于锥形瓶中,加入酚酞作指示剂,用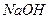 溶液滴定到终点。
溶液滴定到终点。
该同学进行了三次实验,实验数据如下表:
滴定中误差较大的是第 次实验,造成这种误差的可能原因是 (填选项编号)
a、在盛装未知浓度的盐酸之前锥形瓶里面有少量蒸馏水,未烘干
b、滴定管在盛装标准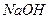 溶液前未润洗
溶液前未润洗
c、滴定开始前盛装标准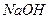 溶液的滴定管尖嘴部分有气泡,滴定终点读数时未发现气泡
溶液的滴定管尖嘴部分有气泡,滴定终点读数时未发现气泡
d、滴定开始前盛装标准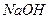 溶液的滴定管尖嘴部分没有气泡,在滴定终点读数时发现尖嘴部分有气泡
溶液的滴定管尖嘴部分没有气泡,在滴定终点读数时发现尖嘴部分有气泡
e、滴定过程中,锥形瓶摇荡得太剧烈,以致有些液滴飞溅出来
f、达到滴定终点时,俯视溶液凹液面最低点读数
g、滴定到终点时,溶液颜色由无色变到了红色
(3)该同学所测得盐酸的物质的量浓度为 (结果保留三位小数)。
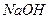 溶液来测定未知浓度的盐酸的浓度:
溶液来测定未知浓度的盐酸的浓度:(1)配制250mL 0.5mol/L的
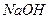 溶液所需的玻璃仪器为 。
溶液所需的玻璃仪器为 。(2)用滴定管准确量取20.00mL未知浓度的盐酸于锥形瓶中,加入酚酞作指示剂,用
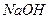 溶液滴定到终点。
溶液滴定到终点。该同学进行了三次实验,实验数据如下表:
| 实验编号 | 盐酸的体积(mL) | 标准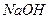 溶液的体积(mL) 溶液的体积(mL) |
| 1 | 20.00 | 18.20 |
| 2 | 17.10 | |
| 3 | 16.90 |
滴定中误差较大的是第 次实验,造成这种误差的可能原因是 (填选项编号)
a、在盛装未知浓度的盐酸之前锥形瓶里面有少量蒸馏水,未烘干
b、滴定管在盛装标准
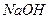 溶液前未润洗
溶液前未润洗c、滴定开始前盛装标准
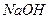 溶液的滴定管尖嘴部分有气泡,滴定终点读数时未发现气泡
溶液的滴定管尖嘴部分有气泡,滴定终点读数时未发现气泡d、滴定开始前盛装标准
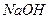 溶液的滴定管尖嘴部分没有气泡,在滴定终点读数时发现尖嘴部分有气泡
溶液的滴定管尖嘴部分没有气泡,在滴定终点读数时发现尖嘴部分有气泡e、滴定过程中,锥形瓶摇荡得太剧烈,以致有些液滴飞溅出来
f、达到滴定终点时,俯视溶液凹液面最低点读数
g、滴定到终点时,溶液颜色由无色变到了红色
(3)该同学所测得盐酸的物质的量浓度为 (结果保留三位小数)。
(1)烧杯、玻璃棒、250mL容量瓶、胶头滴管。(4分)
(2)1,bcg (4分) (3)0.425mol/L (2分)
(2)1,bcg (4分) (3)0.425mol/L (2分)
略

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目
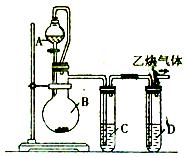
 化学方程式:__________________________。
化学方程式:__________________________。 ____________。
____________。 __(填Ⅰ或Ⅱ)。
__(填Ⅰ或Ⅱ)。
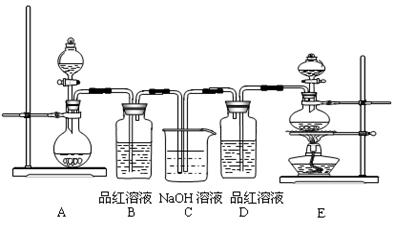
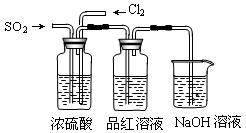
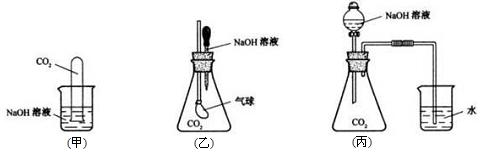

 实验室有以下的仪器和药品可供使用:
实验室有以下的仪器和药品可供使用: 请回答:
请回答: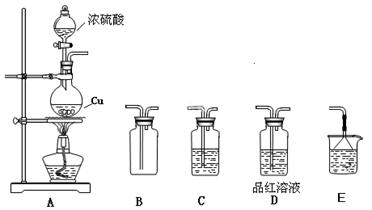
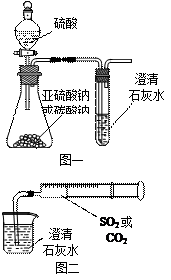
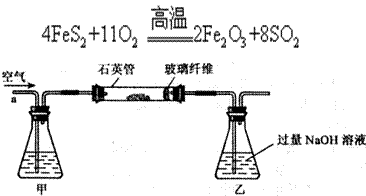
 )进行如下实验探究。
)进行如下实验探究。 g该黄铁矿样品(杂质中不含硫和铁)放入如下图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通人空气,高温灼烧石英管中的黄铁矿样品至反应完全。石英管中发生反应的化学方程式为:
g该黄铁矿样品(杂质中不含硫和铁)放入如下图所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通人空气,高温灼烧石英管中的黄铁矿样品至反应完全。石英管中发生反应的化学方程式为: