��Ŀ����
����Ŀ����һ�������£���������������������·�Ӧ��2SO2(g)+O2(g)![]() 2SO3(g) ��H<0����������֪SO3���۵�Ϊ16.83�棬�е���44.8�档ij��ѧѧϰС����ͨ��ʵ��ⶨ������Ӧ��SO2��ת���ʣ��������������ʵ�顣
2SO3(g) ��H<0����������֪SO3���۵�Ϊ16.83�棬�е���44.8�档ij��ѧѧϰС����ͨ��ʵ��ⶨ������Ӧ��SO2��ת���ʣ��������������ʵ�顣

�����Ҫ��ش����⣺
��1����װ�ýӿڵ�����˳����a��__��
��2��װ�â��ձ���ʢ�ű�ˮ��������__��
��3��װ�â��������ᣬһ��ѡ��Ũ��Ϊ70%��80%�����ᣬԭ����__��
��4����װ�â��з�Ӧ����ʱ��Ҫ��ֹˮ�м���ͨ��O2һ��ʱ�䣬����ͨ��O2��Ŀ����__��
��5������agNa2SO3��ĩ���������ᷴӦ��ʵ�������Ƶ�װ�â�����bg����ʽ��ʾ��ʵ����SO2��ת����__��
���𰸡�h��i��b��c��f��g��d��e ʹSO3�����Ա�������з������ ����Ũ�ȹ���ʱ��Ҫ�Է�����ʽ���ڣ���Ӧ����������Ũ�ȹ�Сʱ���ɵ�SO2�Ჿ���ܽ���ϡ������ ��װ���е�SO2ȫ������װ�����з�����Ӧ����SO3ȫ������װ����������Ϊ���壬��߲���SO2ת���ʵ�ȷ�� ![]()
��������
��1��װ��������������ȡSO2����O2��ϣ�װ�����з���SO2�Ĵ�������Ӧ��װ����������������β����װ�������ռ�SO3��װ�����������Ǹ������壻
��2��SO3���۵�ϵͣ���ͨ���������룻
��3�����ݷ�Ӧԭ��Ϊǿ�������ᣬ��SO2��ˮ���ܽ�Ƚϴ������
��4����Ӧ������װ���л����һ���ֵ�SO2���壻
��5������SԪ���غ���м��㡣
��1����װ�����ӻ���˳��Ϊ����ȡSO2����O2���װ��������SO2��O2װ������ȡSO3װ��������SO3װ����β������װ�ã����װ�ýӿڵ�����˳���ǣ�a��h��i��b��c��f��g��d��e��
��2������SO3���۷е�֪��װ�����ձ���ʢ�ű�ˮ��ʹSO3�����Ա�������з��������
��3������Ũ�ȹ���ʱ������Ҫ�Է�����ʽ���ڣ����Ե���������ӣ���Ӧ����������Ũ�ȹ�Сʱ����Ӧ���ɵ�SO2�Ჿ���ܽ���ϡ�����У����ᵼ��ʵ�������
��4����Ӧ������װ�����л����SO2��װ�����л����SO3����Ӧ��������ͨ������һ��ʱ�䣬���Խ�װ���е�SO2ȫ������װ�����з�����Ӧ����SO3ȫ������װ����������Ϊ���壬����Ӱ��SO2ת���ʵIJⶨ��
��5������Na2SO3ȫ����Ӧ����SO2������SO2�������β������װ�ã�����SԪ���غ��֪����ȫת��ʱ����������SO3������Ϊ![]() ���ʸ�ʵ����SO2��ת����Ϊ
���ʸ�ʵ����SO2��ת����Ϊ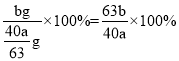 ��
��

����Ŀ���ҹ����ұ���GB2760���涨���Ѿ���SO2���ʹ����Ϊ0��25 g��L-1��ij��ȤС����ͼ1װ�ã��г�װ���ԣ��ռ�ij���Ѿ���SO2�������京�����вⶨ��
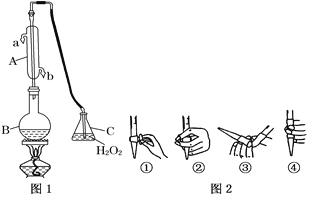
��1������A��������__________��ˮͨ��A�Ľ���Ϊ________��
��2��B�м���300��00 mL���Ѿƺ��������ᣬ����ʹSO2ȫ���ݳ�����C��H2O2��ȫ��Ӧ���仯ѧ����ʽΪ_____________________________��
��3����ȥC�й�����H2O2��Ȼ����0��090 0 mol��L��1NaOH����Һ���еζ����ζ�ǰ������ʱ��Ӧѡ��ͼ2�е�______�����ζ��յ�ʱ��Һ��pH��8��8����ѡ���ָʾ��Ϊ______������50 mL�ζ��ܽ���ʵ�飬���ζ����е�Һ���ڿ̶���10�����������Һ������������ţ�__________���٣�10 mL���ڣ�40 mL���ۣ�10 mL���ܣ�40 mL����
��4���ζ����յ�ʱ������NaOH��Һ25��00 mL�������Ѿ���SO2����Ϊ��________g��L-1��
��5���òⶨ�����ʵ��ֵƫ�ߣ�����ԭ����������װ������Ľ���ʩ�� ____________��
��6�������£���һ������NaOH��Һ�����ݳ���SO2���壬�����պ������Һǡ�ó����ԣ����й��ڸ�����Һ��˵����ȷ����______________________��
A��c��Na+����c��HSO3-����2c��SO32-�� |
B��c��Na+��>c��HSO3-����c��SO32-��>c��H+�� = c��OH-�� |
C��2c��Na+����3c��H2SO3����3c��HSO3-����3c��SO32-�� |
D��c��Na+��>c��HSO3- �� + c��SO32-�� +c��H2SO3�� |