��Ŀ����
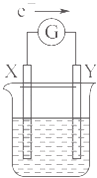
����Ŀ��ijС��ͬѧ���������������������ȷ�Ӧ��õ��Ĺ����������ʵ�飮
��1��������������Ӧ�Ļ�ѧ����ʽ�� ��
��2������ɷֵij���ȷ����
ʵ����� | ���������� |
�� | ȡ����������Ʒ���������ϡ���ᣬ�����ܽ⣬������ɫ���壨������ΪH2������Һ��dz��ɫ |
�� | ����������Һ�м�������KSCN��Һ����Һ��dz��ɫ���ټ���H2O2��Һ��������������ɫ���壨������ΪO2������Һ��Ϊ���ɫ���Һ�ɫ�ܿ���ȥ |
��������ʵ���֪����Һ��FeԪ�صĴ�����ʽ��
�ڢ��в���H2��ԭ������Ʒ�г���Fe�⣬������δ��Ӧ��Al��Ϊ������Ʒ���Ƿ�Al���ʣ���������ʵ�飬���ݵ�ԭ���ǣ������ӷ���ʽ��ʾ��
������O2�Ļ�ѧ����ʽ��
��һ����ʵ�����������������Ʒ��FeԪ�صĴ�����ʽ�У�Fe��Fe2O3��Fe3O4 ��
��3����С��ͬѧ�Ԣ�����Һ��ɫ��ȥ��ԭ������һ��̽����
ʵ����� | ���������� |
�� | ������ʣ����Һ����Ϊ���ݣ�һ�ݵμ�NaOH��Һ���������ɫ������ |
�� | ȡ2mL 0.1mol/L FeCl3��Һ������KSCN��Һ����Һ��Ϊ��ɫ��ͨ��һ��ʱ��O2 �� |
��ʾ��KSCN��SԪ�صĻ��ϼ�Ϊ��2��
��ʵ�颣�а�ɫ�����Ļ�ѧʽ��
�ڽ��ʵ�颣�͢�������ʵ�颢�к�ɫ��ȥ��ԭ����
�۲������ϵ�֪��Cl������Һ��ɫ��ȥ�ķ�Ӧ�д����ã���֤��˵��Ӧ�����ʵ��������� ��
���𰸡�
��1��2Al+Fe2O3 ![]() Al2O3+2Fe
Al2O3+2Fe
��2��Fe2+��Fe3+��2Al+2NaOH+2H2O=2NaAlO2+3H2����2H2O2 ![]() 2H2O+O2��
2H2O+O2��
��3��BaSO4����Һ��SCN�����ӱ�H2O2��������Һ��ɫ��ȥ���ֱ�ȡ2mL0.1mol/LFeCl3��Һ��2mL 0.05mol/L Fe2��SO4��3��Һ���ֱ����KSCN��Һ����Һ����Ϊ��ɫ���ٷֱ�����Ũ�ȵ������H2O2��Һ��FeCl3��Һ��ɫ�죨��ȡ0.05mol/L Fe2��SO4��3��Һ������KSCN��Һ����Һ���ɫ������ɫ��Һ��Ϊ2�ݣ�1�ݼ���NaCl���壬��һ�ݲ��䣬����������Һ�о������Ũ�ȵ������H2O2��Һ������NaCl����Һ��ɫѸ����ɫ��
���������⣺��1��Al���������ڸ����·������ȷ�Ӧ������������������Ӧ�Ļ�ѧ����ʽΪ��2Al+Fe2O3 ![]() Al2O3+2Fe�����Դ��ǣ�2Al+Fe2O3
Al2O3+2Fe�����Դ��ǣ�2Al+Fe2O3 ![]() Al2O3+2Fe����2��������������Һ�м�������KSCN��Һ����Һ��dz��ɫ��˵����Һ�к���Fe3+ �� �ټ���H2O2��Һ��������������ɫ���壨������ΪO2������Һ��Ϊ���ɫ��˵����Һ����˫��ˮ����Һ��������Ũ��������ԭ��Һ�к���Fe2+ ��
Al2O3+2Fe����2��������������Һ�м�������KSCN��Һ����Һ��dz��ɫ��˵����Һ�к���Fe3+ �� �ټ���H2O2��Һ��������������ɫ���壨������ΪO2������Һ��Ϊ���ɫ��˵����Һ����˫��ˮ����Һ��������Ũ��������ԭ��Һ�к���Fe2+ ��
���Դ��ǣ�Fe2+��Fe3+���ڽ������ܹ�������������Һ��Ӧ����ƫ�����ƺ���������Ӧ�Ļ�ѧ����ʽΪ��2Al+2NaOH+2H2O=2NaAlO2+3H2������д�����ӷ���ʽΪ��2Al+2OH��+2H2O=2AlO2��+3H2����������������������Һ��Ӧ���ݴ˿��Լ����Ƿ���Al��
���Դ��ǣ�2Al+2NaOH+2H2O=2NaAlO2+3H2������˫��ˮ�������������������·ֽ�����ˮ����������Ӧ�Ļ�ѧ����ʽΪ��2H2O2 ![]() 2H2O+O2����
2H2O+O2����
���Դ��ǣ�2H2O2 ![]() 2H2O+O2������3��ʵ�颢����Һ��ɫ��ȥ��ԭ���Ȼ��Fe3+��SCN�����������£�ʵ�颣������֤ʵ�颢ʣ�����Һ�д��������ӣ�Ȼ��֤����Һ�д�����������ӣ��Ӷ�֤��SCN����������ʵ�颤֤������SCN������˫��ˮ���������������ټ����Ȼ�����Һ�����ɲ���������İ�ɫ����ΪBaSO4 ��
2H2O+O2������3��ʵ�颢����Һ��ɫ��ȥ��ԭ���Ȼ��Fe3+��SCN�����������£�ʵ�颣������֤ʵ�颢ʣ�����Һ�д��������ӣ�Ȼ��֤����Һ�д�����������ӣ��Ӷ�֤��SCN����������ʵ�颤֤������SCN������˫��ˮ���������������ټ����Ȼ�����Һ�����ɲ���������İ�ɫ����ΪBaSO4 ��
���Դ��ǣ�BaSO4������Һ�д���ƽ�⣺Fe3++3SCN��Fe��SCN��3 �� ����˫��ˮ��SCN����������SCN����Ũ�ȼ�С��ƽ�����������ƶ���������Һ��ɫ��ȥ��
���Դ��ǣ���Һ��SCN�����ӱ�H2O2��������Һ��ɫ��ȥ���۽�ʵ�颤��2mL 0.1mol/L FeCl3��Һ��Ϊ2mL 0.05mol/L Fe2��SO4��3��Һ���ظ���ʵ�飬����Ϊ������˫��ˮ��Һ��ɫ��һ��ʱ����ȥ��������ȥ���������������������Ϊ���ֱ�ȡ2mL 0.1mol/L FeCl3��Һ��2mL 0.05mol/L Fe2��SO4��3��Һ���ֱ����KSCN��Һ����Һ����Ϊ��ɫ���ٷֱ�����Ũ�ȵ������H2O2��Һ��FeCl3��Һ��ɫ�죨��ȡ0.05mol/L Fe2��SO4��3��Һ������KSCN��Һ����Һ���ɫ������ɫ��Һ��Ϊ2�ݣ�1�ݼ���NaCl���壬��һ�ݲ��䣬����������Һ�о������Ũ�ȵ������H2O2��Һ������NaCl����Һ��ɫѸ����ɫ����
���Դ��ǣ��ֱ�ȡ2mL0.1mol/LFeCl3��Һ��2mL 0.05mol/L Fe2��SO4��3��Һ���ֱ����KSCN��Һ����Һ����Ϊ��ɫ���ٷֱ�����Ũ�ȵ������H2O2��Һ��FeCl3��Һ��ɫ�죨��ȡ0.05mol/L Fe2��SO4��3��Һ������KSCN��Һ����Һ���ɫ������ɫ��Һ��Ϊ2�ݣ�1�ݼ���NaCl���壬��һ�ݲ��䣬����������Һ�о������Ũ�ȵ������H2O2��Һ������NaCl����Һ��ɫѸ����ɫ����

 �п�������㾫��ϵ�д�
�п�������㾫��ϵ�д� ������ĩ��ϰ��ѵ��ϵ�д�
������ĩ��ϰ��ѵ��ϵ�д� С��ʿ��ĩ����100��ϵ�д�
С��ʿ��ĩ����100��ϵ�д�