题目内容
15.下列说法正确的是( )①需要加热方能发生的反应一定是吸收能量的反应
②释放能量的反应在常温下一定很容易发生
③反应是释放能量还是吸收能量必须看反应物和生成物所具有的总能量的相对大小
④释放能量的反应加热到一定温度引发后,停止加热反应也能继续进行.
| A. | 只有③④ | B. | 只有①② | C. | ①②③④ | D. | 只有②③④ |
分析 化学反应过程中一定伴随着能量的改变,主要是由反应物的总能量和生成物的总能量的相对大小决定;当反应物的总能量大于生成物的总能量,反应为放热反应;反之则反之;大多数的放热反应进行时需一定的引发条件才能进行.
解答 解:①需要加热方能发生的反应不一定是吸热反应,好多放热反应也需要加热如铝热反应,故①错误;
②放热反应在常温下不一定很容易发生,例如氢气和氧气常温下不会反应,但点燃会瞬间完成,故②错误;
③反应物的总能量和生成物的总能量的相对大小决定反应是吸热反应还是放热反应,故③正确;
④放热反应引发后利用放出的热量可以保持反应继续进行,故④正确,
故选A.
点评 本题考查化学反应的能量变化与反应物的总能量和生成物的总能量有关,放热反应、吸热反应的进行条件,题目较简单.

练习册系列答案
相关题目
5.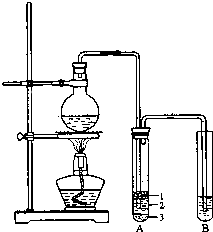 某化学兴趣小组的同学为制取少量溴乙烷,查阅资料得知:
某化学兴趣小组的同学为制取少量溴乙烷,查阅资料得知:
NaBr+H2SO4→HBr+NaHSO4
CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O
化学兴趣小组根据实验原理设计如图的装置.根据题意完成下列填空:有关数据列表如下:
(1)圆底烧瓶中加入的反应物是溴化钠、乙醇和2:1的硫酸.配制体积比2:1的硫酸所用的仪器为abc选填编号)
a.烧杯 b.玻璃棒 c.量筒 d.容量瓶 e.滴定管
(2)将生成物导入盛有冰水混合物的试管A中,试管A中的物质分为三层(如图所示),产物在第3层;
(3)用浓的硫酸进行实验,若试管A中获得的有机物呈棕黄色,除去其中杂质应加入d选填编号)然后再进行分液一步操作即可;
a.无水氯化钙 b.硝酸银溶液 c.四氯化碳 d.亚硫酸钠溶液
(4)实验过程中,同学发现仪器连接部分有漏气现象,老师建议把上述装置中的仪器连接部分都改成标准玻璃接口,其原因是:反应会产生Br2,腐蚀橡胶;
(5)假设最初取用的无水乙醇是57.5mL,最后得到的纯净的溴乙烷是52.0mL,则溴乙烷的产率为66.8%.
 某化学兴趣小组的同学为制取少量溴乙烷,查阅资料得知:
某化学兴趣小组的同学为制取少量溴乙烷,查阅资料得知:NaBr+H2SO4→HBr+NaHSO4
CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O
化学兴趣小组根据实验原理设计如图的装置.根据题意完成下列填空:有关数据列表如下:
| 乙醇 | 溴乙烷 | |
| 状态 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.8 | 1.4 |
| 沸点/℃ | 78.5 | 119.0 |
| 熔点/℃ | -130 | 38.4 |
a.烧杯 b.玻璃棒 c.量筒 d.容量瓶 e.滴定管
(2)将生成物导入盛有冰水混合物的试管A中,试管A中的物质分为三层(如图所示),产物在第3层;
(3)用浓的硫酸进行实验,若试管A中获得的有机物呈棕黄色,除去其中杂质应加入d选填编号)然后再进行分液一步操作即可;
a.无水氯化钙 b.硝酸银溶液 c.四氯化碳 d.亚硫酸钠溶液
(4)实验过程中,同学发现仪器连接部分有漏气现象,老师建议把上述装置中的仪器连接部分都改成标准玻璃接口,其原因是:反应会产生Br2,腐蚀橡胶;
(5)假设最初取用的无水乙醇是57.5mL,最后得到的纯净的溴乙烷是52.0mL,则溴乙烷的产率为66.8%.
3.如图是A、B、C三种物质的溶解度曲线,下列有关说法正确的是( )
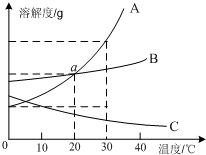

| A. | a点溶液A、B的物质的量浓度相等 | |
| B. | 通常采用降温结晶的方法获得晶体B | |
| C. | 用蒸发浓缩、趁热过滤从C的溶液中分离出晶体C | |
| D. | 30℃时,A的饱和溶液的质量分数约为35% |
10.利用下表提供的仪器、试剂,就能达到相应实验目的是( )
| 选项 | 仪器 | 试剂 | 实验目的 |
| A | 托盘天平(带砝码)、滴管、量筒、烧杯、药匙、玻璃棒 | 食盐,蒸馏水 | 配制一定物质的量浓度的NaCl溶液 |
| B | 烧杯、漏斗、滴管、铁架台(带铁圈)、玻璃棒、滤纸、导气管 | 烧碱,CO2,稀盐酸 | 除去AlCl3溶液中少量的MgCl2 |
| C | 酸式滴定管、滴管、铁架台(带铁夹) | 已知浓度的盐酸、石蕊 | 测定NaOH溶液的浓度 |
| D | 分液漏斗、烧瓶、锥形瓶、导管、橡皮塞 | 稀盐酸,大理石,硅酸钠溶液 | 证明非金属性:Cl> C>Si |
| A. | A | B. | B | C. | C | D. | D |
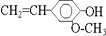 ,它不可能具有的性质是( )
,它不可能具有的性质是( )