题目内容
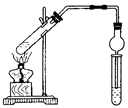
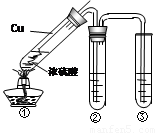
 用右图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应的产物,下列有关说法正确的是( )
用右图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应的产物,下列有关说法正确的是( )分析:A、根据浓硫酸中元素的化合价是否变化判断.
B、品红溶液是检验二氧化硫的存在.
C、根据二氧化硫和氯化钡是否反应分析.
D、根据铜与浓硫酸反应的现象分析.
B、品红溶液是检验二氧化硫的存在.
C、根据二氧化硫和氯化钡是否反应分析.
D、根据铜与浓硫酸反应的现象分析.
解答:解:A、浓硫酸和铜反应生成硫酸铜、二氧化硫和水,所以部分硫酸有化合价的变化,部分硫酸化合价不变,所以浓硫酸既表现了强氧化性,又表现了酸性,故A正确.
B、SO2具有漂白性,可用品红溶液验证SO2的生成,故B正确;
C、二氧化硫溶于水生成的亚硫酸是弱酸,所以亚硫酸和氯化钡不反应;SO2为酸性气体,具有污染性,可与碱发生反应,可用NaOH溶液吸收多余的SO2,故C错误.
D、铜与浓硫酸的反应实验中,铜丝与过量浓硫酸的反应生成是硫酸铜,试管中含有大量水,不会生成白色固体,故D错误.
故选A.
B、SO2具有漂白性,可用品红溶液验证SO2的生成,故B正确;
C、二氧化硫溶于水生成的亚硫酸是弱酸,所以亚硫酸和氯化钡不反应;SO2为酸性气体,具有污染性,可与碱发生反应,可用NaOH溶液吸收多余的SO2,故C错误.
D、铜与浓硫酸的反应实验中,铜丝与过量浓硫酸的反应生成是硫酸铜,试管中含有大量水,不会生成白色固体,故D错误.
故选A.
点评:本题考查了铜与浓硫酸反应的实验,难度较大,易错选项是D,注意二氧化硫和次氯酸漂白原理的区别.

练习册系列答案
 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目
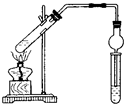 用右图所示实验装置制取乙酸乙酯.回答以下问题:
用右图所示实验装置制取乙酸乙酯.回答以下问题: A.上下移动①中铜丝可控制
A.上下移动①中铜丝可控制