��Ŀ����
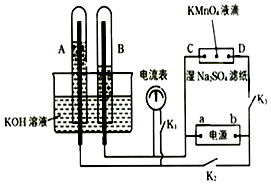
����Ŀ��ij�о���ѧϰС���ù�ҵ̼��ƣ���Ҫ�ɷ�ΪCaCO3������Ϊ��Al2O3��FeCO3�� Ϊԭ�ϣ����Ʊ������Σ������������Һ�����ȡ����ƣ������ͼ�������ʵ��ܽ������������ؽ������������������������pH����ʼ������pH����������Ũ��Ϊ1.0molL��1���㣩�����ṩ���Լ��У�a�������ƣ�b.5molL��1���ᣬc.5molL��1���ᣬd.5molL��1���ᣬe.3%H2O2��Һ��f������ʯ��ˮ��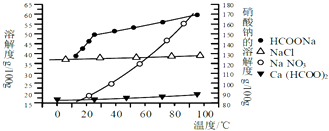
�������� | ��ʼ������pH | ������ȫ��pH |
Fe3+ | 1.1 | 3.2 |
Al3+ | 3.0 | 5.0 |
Fe2+ | 5.8 | 8.8 |
�벹��������̼����Ʊ�����Ƶ�ʵ�鲽��
����1����ȡ13.6g����������Լ20mLˮ�������Һ���ã�����ȡ��ϸ��̼�����Ʒ10g���ã�
����2�� ��
����3�� ��
����4�����˺���Һ���������Һ��ϣ�������ҺpH 7��8����ֽ��裬������Һ������ϴ�Ӹ���ü���ƾ��壮
���𰸡����Թ��������ܽ�̼�����Ʒ����ʯ��ˮ������ҺpH=5������Ũ���������ᾧ�������ȹ���
����������ʵ������Ҫȥ�����ʣ�ͬʱ���ɿ����Ը��Σ�������������������Ҫ����Ϊ�����ӣ�˫��ˮ�����ᣩ������������������ȥ��������ҲҪ���ɼ��ȥ���ʵ���pHΪ5����ʯ��ˮ���ڣ���Ȼ������������Һ��������ܽ�Ƚ�С�����¶ȱ仯�������Ǽ���ƣ�������Ũ�����õ�����ƹ��壬���ȹ��ˣ���ֹ�������������������IJ���Ϊ������1����ȡ13.6g����������Լ20mLˮ�������Һ���ã�����ȡ��ϸ��̼�����Ʒ10g���ã��������ǿ�����ԣ��������ܽ����ʣ����������������ӣ�Ϊ��һ����������ת��������������������������������������ԣ�����ѡ�ã���������ܣ�������������ϡ����������������������Բ�ѡ�����ԣ�����2�����Թ��������ܽ�̼�����Ʒ����������������ȫ��pH=3.2������������������ȫ��pH=5��������ҺpH=5������������������������������ȥ�����ԣ�����3����ʯ��ˮ������ҺpH=5��ͨ�������ᾧ�����ȹ��ˣ���ֹ�����������������ԣ�����4�����˺���Һ���������Һ��ϣ�������ҺpH 7��8����ֽ��裬������Һ������Ũ�������ȹ��ˡ�ϴ�ӡ�60��ʱ����ü���ƾ��壬���Դ��ǣ����Թ��������ܽ�̼�����Ʒ����ʯ��ˮ������ҺpH=5������Ũ���������ᾧ�������ȹ��ˣ�