题目内容
某元素的一种同位素X的原子质量数为A,含N个中子,它与1H原子组成1HmX分子,在a g 1HmX中所含质子的物质的量是
A.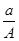 (A-N+m)mol (A-N+m)mol | B.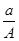 (A-N)mol (A-N)mol |
C.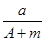 (A-N)mol (A-N)mol | D.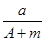 (A-N+m)mol (A-N+m)mol |
D
解析试题分析:X的原子质量数为A,含N个中子,则X的质子数是A-N,agHmX的物质的量是a/(m+A)mol,所以其分子中含有的质子的物质的量是a/(m+A) ×(m+A-N)mol=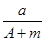 (A-N+m)mol,答案选D。
(A-N+m)mol,答案选D。
考点:考查质量数、质子数、中子数的关系,物质的量的有关计算

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
下列元素中,属于第三周期IVA族的是
| A.钠 | B.镁 | C.硅 | D.硫 |
短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13。X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者Y原子最外层电子数的3倍。下列说法正确的是
| A.X的氢化物溶于水显酸性 | B.Y的氧化物是共价化合物 |
| C.其离子半径大小: Z>Y>X | D.X和Z的最高价氧化物对应的水化物都是强酸 |
(原创)短周期元素X、Y、Z、W、Q在元素周期表中的位置如表所示,其中W的气态氢化物摩尔质量为34g/mol,Y的最低价氢化物为非电解质。则下列说法中正确的是
| | X | Y | |
| Z | | W | Q |
A.阴离子还原性:W > Q
B.X的最低价氢化物能形成分子间氢键
C.Q单质能溶于水,且水溶液须用棕色细口瓶盛装
D.Na与Y能形成化合物Na2Y2,且与水反应后溶液呈碱性
元素在周期表中的位置,反映了元素的原子结构和元素的性质。下列说法正确的是( )
| A.同一元素不可能既表现金属性,又表现非金属性 |
| B.第三周期元素的最高正化合价等于它所处的主族序数 |
| C.短周期元素形成离子后,最外层都达到8电子稳定结构 |
| D.同一主族的元素的原子,最外层电子数相同,化学性质完全相同 |
下列原子中未成对电子数为3的是
| A.O | B.N | C.F | D.Cu |
核电荷数小于l8的某元素X,其原子的电子层数为n,最外层电子数为(2n+1),
原子核内质子数为(2n2一1)。下列关于元素X的说法中,不正确的是( )
| A.其最高化合价一定为+5 | B.可以形成化学式为KXO3的盐 |
| C.其氢化物可以用来做喷泉实验 | D.其最高价氧化物的水化物是强酸 |
电子层数相同的三种元素X、Y、Z,已知最高价氧化物对应水化物的酸性HXO4、H2YO4、H3ZO4,则下列判断错误的是 ( )
| A.原子半径X>Y>Z | B.气态氢化物的稳定性HX>H2Y>ZH3 |
| C.非金属性X>Y>Z | D.气态氢化物的还原性HX<H2Y<ZH3 |
下表是部分短周期元素的原子半径及主要化合价,根据表中的信息,判断下面叙述正确的是
| 元素代号 | L | M | Q | R | T |
| 原子半径(nm) | 0.160 | 0.143 | 0.089 | 0.102 | 0.074 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
B.M与T形成的化合物具有两性
C.单质与同浓度的稀盐酸反应的速率为Q>L
D.R与T的氢化物熔沸点高低为H2R>H2T