题目内容
电子层数相同的三种元素X、Y、Z,已知最高价氧化物对应水化物的酸性HXO4、H2YO4、H3ZO4,则下列判断错误的是 ( )
| A.原子半径X>Y>Z | B.气态氢化物的稳定性HX>H2Y>ZH3 |
| C.非金属性X>Y>Z | D.气态氢化物的还原性HX<H2Y<ZH3 |
A
解析试题分析:同一周期的元素,元素的原子序数越大,元素的非金属性就越强,其最高价氧化物对应水化物的酸性就越强。元素的原子半径就越小,其简单的氢化物的稳定性就越强,还原性就越弱。酸性:HXO4 >H2YO4>H3ZO4,所以A.原子半径X<Y<Z ,错误;B.气态氢化物的稳定性HX>H2Y>ZH3,正确;C.非金属性X>Y>Z ,正确;D.气态氢化物的还原性HX<H2Y<ZH3,正确。
考点:考查元素的性质与原子结构、元素在周期表中的位置的关系的知识。

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
下列有关元素周期表的说法中,正确的是
| A.能生成碱的金属元素都在ⅠA族 |
| B.原子序数为14的元素位于元素周期表的第3周ⅥA族 |
| C.稀有气体元素原子的最外层电子数为2或8 |
| D.元素周期表有18个纵行,分列16个族,即7个主族、8个副族和1个0族 |
某元素的一种同位素X的原子质量数为A,含N个中子,它与1H原子组成1HmX分子,在a g 1HmX中所含质子的物质的量是
A.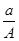 (A-N+m)mol (A-N+m)mol | B.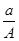 (A-N)mol (A-N)mol |
C.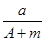 (A-N)mol (A-N)mol | D.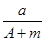 (A-N+m)mol (A-N+m)mol |
下列元素中,最高正化合价数值最大的是
| A.Na | B.P | C.C1 | D.C |
根据元素周期表和元素周期律分析,下列推断中错误的是( )
| A.铍的原子失去电子能力比镁弱 | B.砹的氢化物不稳定 |
| C.硒化氢比硫化氢稳定 | D.氢氧化锶比氢氧化钙的碱性强 |
决定原子种类的因素是
| A.质子数和中子数 | B.质子数 | C.电子数 | D.质子数和电子数 |
下列选项中与主族元素在元素周期表中所处的位置相关的是
| A.相对原子质量 | B.核内中子数 |
| C.次外层电子数 | D.电子层数和最外层电子数 |
今年5月7日某公司丢失铱-192放射源的事件再次敲响核安全的警钟。下列关于铱-192 (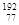 Ir)的说法正确的是
Ir)的说法正确的是
| A.原子序数为77 | B.电子数为115 | C.中子数为192 | D.质量数为77 |