��Ŀ����
����Ŀ�������������ֿ��������쵼�����״��ֺ��Աʹ�õ�����ƿ���Ʊ�����һ���䷽�к��������������ʣ�

��д���пհף�
(1) ���в�����ԭ�ӵĹ�����������__________�������Լ������Ӧ����ɫ����__________ (���ţ���
a. Br2/CCl4��Һ b.ʯ����Һ c.����KMnO4��Һ
(2) ��ͬ���칹���ж��֣�д������һ�ֲ�����������Ľṹ��ʽ____________
(3) ����ͨ������ת�����Եõ���(C2H6O2)(����AD��Ϊ�л��AΪһ�ֵ��ǣ�BΪһ����������ζ��һԪ����CΪһ�����壩
![]()
Bת�����ҵ�һϵ�з�Ӧ���漰���ķ�Ӧ������__________��
a.��ȥ��Ӧ b.ȡ����Ӧ
c.�ӳɷ�Ӧ d.�Ӿ۷�Ӧ
Bת��ΪC�Ļ�ѧ��Ӧ����ʽΪ______________________________
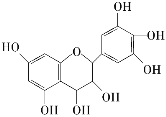
(4) �����ﶡ����̼���⡢������Ԫ�أ�����Է�������Ϊ110������FeCl3��Һ����������ɫ���Ҷ������б����ϵ�һ��ȡ����ֻ��һ�֡��Ľṹ��ʽΪ______________
(5) ��֪��![]()
![]()
����������Ϣ���Ա�����ϩ���Ȼ���Ϊԭ�Ͼ�������Ӧ�ϳɱ�����������ȡ����Ӧ�Ļ�ѧ����ʽ��________________________
���𰸡�̼̼˫������![]() �� ac CH2=CH-CH2-CH2-COOH abc CH3CH2OH
�� ac CH2=CH-CH2-CH2-COOH abc CH3CH2OH![]() CH2 = CH2��+ H2O
CH2 = CH2��+ H2O ![]()
![]()
��������
(1)���к�C=C��-COOC-����C=C�ܷ����ӳɺ�������Ӧ��
(2)��ͬ���칹����һ�ֲ����������ᣬ��C=C��-COOH��
(3)����ˮ��õ�AΪ�����ǣ�������ת�������Ҵ����Ҵ�������ȥ��Ӧ������ϩ����ϩ���巢���ӳɷ�Ӧ����1��2-�������飬1��2-��������ˮ�������Ҷ�����
(4)��Է�������Ϊ110�������з��ǻ���110-12��6-6-16=16����2����-OH���������������ϵ�һ��ȡ����ֻ��һ�֣���ṹ�Գƣ���-OHλ�ڶ�λ��
(5)�Ա�����ϩ���Ȼ���Ϊԭ�Ͼ�������Ӧ�ϳɱ�����ϩ�ӳ����������飬���������鷢��ȡ����Ӧ���ɱ����飬�����ȥ���ɱ���
(1)���к�C=C��-COOC-������Ϊ̼̼˫��(��![]() )�����������в��������Ĺ�����Ϊ̼̼˫��(��
)�����������в��������Ĺ�����Ϊ̼̼˫��(��![]() )����C=C�ܷ����ӳɺ�������Ӧ����ac�����ʷ�Ӧ��ɫ��
)����C=C�ܷ����ӳɺ�������Ӧ����ac�����ʷ�Ӧ��ɫ��
(2)��ͬ���칹����һ�ֲ����������ᣬ��C=C��-COOH����ṹ��ʽΪCH2=CH-CH2-CH2-COOH��
(3)����ˮ������AΪ�����ǣ�������ת�������Ҵ����Ҵ�������ȥ��Ӧ������ϩ����ϩ��������Ȼ�̼��Һ�����ӳɷ�Ӧ����1��2-�������飬1��2-��������ˮ�������Ҷ�������Bת�����ҵ�һϵ�з�Ӧ���漰���ķ�Ӧ��������ȥ��Ӧ���ӳɷ�Ӧ��ȡ����Ӧ���ʴ�Ϊabc������Bת��ΪCΪ�Ҵ�����ȥ��Ӧ����Ӧ����ʽΪCH3CH2OH![]() CH2 = CH2��+ H2O��
CH2 = CH2��+ H2O��
(4)��Է�������Ϊ110�������з��ǻ���110-12��6-6-16=16����2����-OH���������������ϵ�һ��ȡ����ֻ��һ�֣���ṹ�Գƣ���-OHλ�ڶ�λ����ṹ��ʽΪ![]() ��
��
(5)��ϩ��HCl�����ӳɷ�Ӧ����CH3CH2Cl������Ϣ��֪������CH3CH2Cl����ȡ����Ӧ�����ұ����ұ��ڴ����������·�����ȥ��Ӧ���ɱ���ϩ������ȡ����Ӧ�Ļ�ѧ����ʽΪ��![]() ��
��

����Ŀ���ϳ�������Ҫ�ɷ���һ����̼�������������ںϳɶ����ѵ����ȼ�ϡ�����Ȼ����úϳ��������п��ܷ����ķ�Ӧ�У�
CH4(g)+H2O(g)![]() CO(g)+3H2(g) ��H1=+206.1kJ/mol ��
CO(g)+3H2(g) ��H1=+206.1kJ/mol ��
CH4(g)+CO2(g)![]() 2CO(g)+2H2(g) ��H2=+247.3kJ/mol ��
2CO(g)+2H2(g) ��H2=+247.3kJ/mol ��
��ش��������⣺
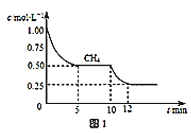
(1)��һ�ܱ������н��з�Ӧ�٣����CH4�����ʵ���Ũ���淴Ӧʱ��ı仯��ͼ1��ʾ����Ӧ���е�ǰ5min�ڣ�v(H2)=____��10minʱ���ı���������������_____��
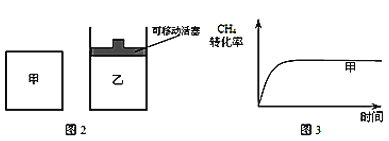
(2)��ͼ2��ʾ���ڼס����������зֱ��������ʵ�����CH4��CO2��ʹ�ס�����������ʼ�ݻ���ȡ�����ͬ�¶��·�����Ӧ�ڣ���ά�ַ�Ӧ�������¶Ȳ��䡣��֪��������CH4��ת������ʱ��仯��ͼ����ͼ3��ʾ������ͼ3�л�����������CH4��ת������ʱ��仯��ͼ��_____��
(3)800��ʱ����ӦCO(g)+H2O(g)![]() CO2(g)+H2(g)�Ļ�ѧƽ�ⳣ��K=1.0��ijʱ�̲�ø��¶��µ��ܱ������и����ʵ����ʵ������±�����ʱ��Ӧ�������淴Ӧ���ʵĹ�ϵʽ��____������ţ���
CO2(g)+H2(g)�Ļ�ѧƽ�ⳣ��K=1.0��ijʱ�̲�ø��¶��µ��ܱ������и����ʵ����ʵ������±�����ʱ��Ӧ�������淴Ӧ���ʵĹ�ϵʽ��____������ţ���
a.v(��)��v(��)
b.v(��)��v(��)
c.v(��)=v(��)
d.���ж�
CO | H2O | CO2 | H2 |
0.5mol | 8.5mol | 2.0mol | 2.0mol |
(4)�����ѣ�CH3OCH3�����ɺϳ�����CO��H2����һ���������Ƶã�д���÷�Ӧ�Ļ�ѧ����ʽ��____��
(5)�Զ����ѡ�����������������ҺΪԭ�ϣ�ʯīΪ�缫����ȼ�ϵ�ء��õ�صĸ����缫��Ӧ����ʽ�ǣ�____���ö�����ȼ�ϵ��Ϊ��Դ���ò��缫���KCl��CuSO4�Ļ����Һ������·��ͨ��0.3mol���ӵĵ���ʱ����������������2.8L������(��״��)����������Һ���Ϊ1L������������ijɷּ����ʵ���Ϊ��____��