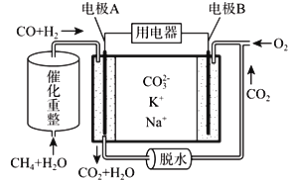
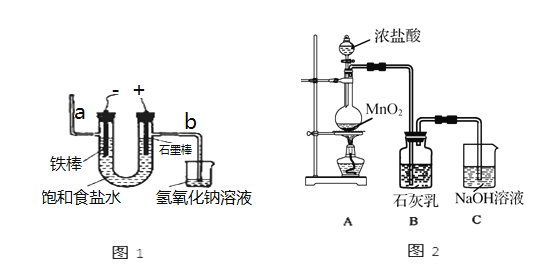
题目内容
【题目】冬日,雪花漫舞,银装素裹,给人们带来美的享受,但降雪却会给道路通行带来麻烦。现有一种高速公路的绿色融雪剂——CMA(醋酸钙、醋酸镁固体混合物),其生产常以白云石(主要成分MgCO3·CaCO3,含SiO2等杂质)和生物质废液——木醋液(主要成分乙酸,以及少量的甲醇、苯酚、焦油等杂质)等为原料,流程如图:
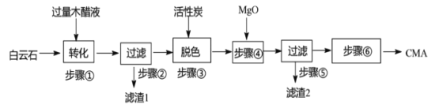
(1)步骤①发生的反应离子方程式为____。
(2)滤渣1的主要成分与NaOH溶液反应的热化学方程式为___(己知与l mol NaOH发生反应时放出热量为QkJ)。步骤②所得滤液常呈褐色,分析可知其原因主要是木醋液中含有少量的有色的焦油以及____。
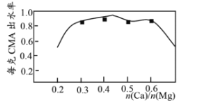
(3)已知CMA中钙、镁的物质的量之比与出水率(与融雪效果成正比)关系如图所示,步骤④的目的除调节n(Ca)∶n(Mg)约为__(选填:A.1∶3;B.1∶2;C.3∶7;D.2∶3)外,另一目的是___。
(4)步骤⑥包含的操作有___、过滤、洗涤及干燥。
(5)取akg含MgCO3·CaCO3质量分数为b%的白云石,经过上述流程制备CMA。已知MgCO3·CaCO3的损失率为c%,步骤④之后到产品CMA的损失率为d%,则结合(3)可知所得产品质量约为____kg(请用含相关字母的计算式表达,不必化简)。
【答案】MgCO3·CaCO3+4CH3COOH=Ca2++Mg2++4CH3COO-+2CO2↑+2H2O SiO2(s)+2NaOH(aq)=Na2SiO3(aq)+H2O(l) △H=-2QkJ/mol 苯酚 C 除去过量的乙酸 蒸发结晶 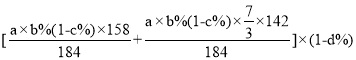
【解析】
根据流程图可知,白云石(主要成分MgCO3CaCO3,含SiO2等杂质)与木醋液(主要成分乙酸)反应生成醋酸钙和醋酸镁,过滤得滤渣1为二氧化硅,滤液中主要溶质是醋酸钙和醋酸镁,加入活性碳脱色,再加入氧化镁,调节溶液中n(Ca):n(Mg)的值,过滤,除去混合液中固体杂质,得醋酸钙和醋酸镁溶液,将滤液蒸发结晶、过滤、洗涤及干燥得CMA,据此判断。
(1)步骤①发生的反应是醋酸溶解白云石,反应的离子方程式为MgCO3CaCO3+4CH3COOH=Ca2++Mg2++4CH3COO-+2CO2↑+2H2O;
(2)己知lmolNaOH与二氧化硅发生反应时放出热量为QkJ,则反应的热化学方程式为Si02(s)+2NaOH(aq)=Na2SiO3(aq)+H2O(l)△H=-2QkJ/mol,步骤②所得滤液常呈褐色,颜色除与木醋液中含有少量的有色的焦油有关外,产生颜色的另一主要原因是实验过程中苯酚被空气中氧气氧化最终产生褐色物质;
(3)根据如图2所示钙、镁的物质的量之比与出水率(与融雪效果成正比)关系,可知,当n(Ca):n(Mg)约为3:7时,出水率最高,所以步骤④的目的除调节n(Ca):n(Mg)约为3:7,步骤④中加入氧化镁的目的是调节钙、镁离子的物质的量之比,除去过量的乙酸;
(4)根据上面的分析可知,步骤⑥包含的操作有蒸发结晶、过滤、洗涤及干燥;
(5)取akg含MgCO3CaCO3质量分数为b%的白云石,经过上述流程制备CMA。已知MgCO3CaCO3的损失率为c%,则可得n[Ca(CH3COO)2]=![]() ×103mol,n[Mg(CH3COO)2]=
×103mol,n[Mg(CH3COO)2]=![]() ×103×
×103×![]() mol,步骤④之后到产品CMA的损失率为d%,则可知所得产品质量约为[
mol,步骤④之后到产品CMA的损失率为d%,则可知所得产品质量约为[![]() +
+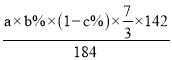 ]×(1-d%)。
]×(1-d%)。