题目内容
【题目】硫化碱法是工业上制备Na2S2O3的方法之一。某研究小组在实验室用硫化碱法制备Na2S2O3·5H2O。
(1)利用吸硫装置A制取Na2S2O3。
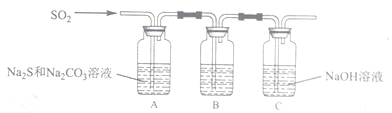
①写出吸硫装置A中发生反应的化学方程式_______________________。
②装置B的作用是检验装置中SO2的吸收效率,B中试剂是_____________,表明SO2吸收效率低的实验现象是B 中溶液___________________ 。
③为了使SO2尽可能吸收完全,除了及时搅拌反应物外,还可采取的合理措施是___________(写出一条即可)。
(2)从反应液中获得Na2S2O3·5H2O晶体的方法是_____________,减压抽滤,洗涤干燥。
(3)实验制得的Na2S2O3·5H2O产品中可能含有Na2SO3、Na2SO4等杂质。请设计实验检测Na2S2O3·5H2O产品中是否存在Na2SO4杂质,简要说明实验操作现象和结论:__________________________。
(4)①Na2S2O3溶液是定量实验中的常用试剂,测定其浓度的过程如下:
第一步:准确称取agKIO3(相对分子质量:214)固体配成溶液;
第二步:加入过量KI固体和H2SO4溶液,滴加指示剂;
第三步:用Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液的体积为VmL
则c(Na2S2O3)=________mol·L-1 (列出算式即可)。
(已知:IO3-+5I-+6H+=3I2+3H2O,2S2O32-+I2= S4O62-+2I-)
②在滴定过程中下列实验操作会造成实验结果偏低的是_______。
A.滴定管未用Na2S2O3溶液润洗
B.滴定终点时仰视读数
C.锥形瓶用蒸馏水润洗后未进行干燥处理
D.滴定管尖嘴处滴定前无气泡,满定终点发现有气泡
【答案】 2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2 品红、溴水或酸性KMnO4溶液 溶液颜色很快褪色(其他合理答案即可) 控制SO2的流速或增大反应物的浓度 蒸发浓缩、降温结晶 取制得的Na2S2O35H2O产品少量于试管中,加水溶解再加入稀盐酸调至酸性,静置片刻,再取上层溶液于试管中,加入BaCl2溶液,有白色沉淀产生,则证明含Na2SO4杂质,否则不含Na2SO4 6000a/214V或 3000a/107V AB
【解析】(1)①吸硫装置A中反应物是二氧化硫、硫化钠和碳酸钠,生成物有硫代硫酸钠,根据原子守恒可知还有二氧化碳生成,因此发生反应的化学方程式为2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2。②二氧化硫具有漂白性,则可以用品红溶液检验SO2的吸收效率,因此B中试剂是品红溶液,表明SO2吸收效率低的实验现象是B中溶液颜色很快褪色。③为了使SO2尽可能吸收完全,除了及时搅拌反应物外,还可采取的合理措施为控制SO2的流速或增大反应物的浓度等。(2)根据后续的实验操作可以判断从反应液中获得Na2S2O3·5H2O晶体的方法是蒸发浓缩、降温结晶,减压抽滤,洗涤干燥。(3)一般利用硫酸钡不溶于水也不溶于酸的性质检验硫酸盐,但需要防止其他离子的干扰,由于硫代硫酸钠能干扰,因此实验操作为:取制得的Na2S2O35H2O产品少量于试管中,加水溶解再加入稀盐酸调至酸性,静置片刻,再取上层溶液于试管中,加入BaCl2溶液,有白色沉淀产生,则证明含Na2SO4杂质,否则不含Na2SO4;(4)①根据方程式可知KIO3~3I2~6Na2S2O3,因此c(Na2S2O3)=![]() mol·L-1;②A.滴定管未用Na2S2O3溶液润洗,浓度减小,消耗标准液体积增加,测定结果偏低;B.滴定终点时仰视读数,读数偏大,消耗标准液体积增加,测定结果偏低;C.锥形瓶用蒸馏水润洗后未进行干燥处理不影响;D.滴定管尖嘴处滴定前无气泡,满定终点发现有气泡,消耗标准液体积减少,浓度偏高,答案选AB。
mol·L-1;②A.滴定管未用Na2S2O3溶液润洗,浓度减小,消耗标准液体积增加,测定结果偏低;B.滴定终点时仰视读数,读数偏大,消耗标准液体积增加,测定结果偏低;C.锥形瓶用蒸馏水润洗后未进行干燥处理不影响;D.滴定管尖嘴处滴定前无气泡,满定终点发现有气泡,消耗标准液体积减少,浓度偏高,答案选AB。

 阅读快车系列答案
阅读快车系列答案