题目内容
下列有关电解质溶液的说法正确的是
| A.在蒸馏水中滴加浓H2SO4,KW不变 |
| B.CaCO3难溶于稀硫酸,也难溶于醋酸 |
| C.在Na2S稀溶液中,c(H+)=c(OH-)-2c(H2S)-c(HS-) |
| D.NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 |
C
浓H2SO4溶于水,放热,温度升高,KW增大,A错误;CaCO3能与CH3COOH发生反应:CaCO3+2CH3COOH=Ca(CH3COO)2+CO2↑+H2O,生成了易溶于水的乙酸钙,所以CaCO3能溶于醋酸,B错误;在Na2S溶液中存在着
电荷守恒:c(H+)+c(Na+)=c(OH-)+c(HS-)+2c(S2-)①
物料守恒:c(Na+)=2[c(S2-)+c(HS-)+c(H2S)]②
①—②可得c(H+)=c(OH-)-2c(H2S)-c(HS-),C正确;由于CH3COO-和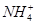 的水解促进了水的电离且促进程度相同,而Na+和Cl-不发生水解,故NaCl溶液中水的电离程度小于CH3COONH4溶液中水的电离程度,D错误。
的水解促进了水的电离且促进程度相同,而Na+和Cl-不发生水解,故NaCl溶液中水的电离程度小于CH3COONH4溶液中水的电离程度,D错误。
电荷守恒:c(H+)+c(Na+)=c(OH-)+c(HS-)+2c(S2-)①
物料守恒:c(Na+)=2[c(S2-)+c(HS-)+c(H2S)]②
①—②可得c(H+)=c(OH-)-2c(H2S)-c(HS-),C正确;由于CH3COO-和
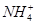 的水解促进了水的电离且促进程度相同,而Na+和Cl-不发生水解,故NaCl溶液中水的电离程度小于CH3COONH4溶液中水的电离程度,D错误。
的水解促进了水的电离且促进程度相同,而Na+和Cl-不发生水解,故NaCl溶液中水的电离程度小于CH3COONH4溶液中水的电离程度,D错误。
练习册系列答案
相关题目
 CO2(g)+H2(g) △H<0。在850℃时,平衡常数K=1。
CO2(g)+H2(g) △H<0。在850℃时,平衡常数K=1。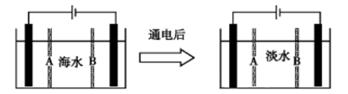

 2NH3(g)ΔH=-92.4 kJ·mol-1,
2NH3(g)ΔH=-92.4 kJ·mol-1,