题目内容
【题目】I:氧化还原反应中实际上包含氧化和还原两个过程.下面是一个还原过程的反应式:NO3-+4H++3e-=NO+2H2O ,已知Cu2O(甲)能使上述还原过程发生.
(1)写出并配平该氧化还原反应的方程式:__________________________________.
(2)反应中硝酸体现了____________、__________性质.
(3)若1mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是__________.
II:现向含6 mol KI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量的关系如图所示。
已知①BrO3-+6I一+6H+=3I2+Br-+3H2O;②2BrO3- +I2 = 2IO3- + Br2;请回答下列问题:
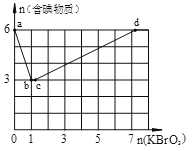
(4)b→c过程中只有一种元素的化合价发生变化,写出该过程的离子反应方程式______。
(5)含6 mol KI的硫酸溶液所能消耗n(KBrO3)的最大值为___________mol。
(6)n(KBrO3)=4时,对应含碘物质的化学式为___________________。
【答案】14HNO3+3Cu2O=6Cu(NO3)2+2NO↑+7H2O 酸性 氧化性 使用了较浓的硝酸,产物中有部分二氧化氮生成 BrO3-+5Br-+6H+=3Br2+3H2O 7.2 I2,KIO3
【解析】
本题主要是考察氧化还原的综合应用,包括方程的配平,图像分析及关系式计算,在配平方程式时要紧抓得失电子守恒。
I(1)根据已知的还原过程和氧化过程的反应物可与推导出,Cu2O会被氧化成![]() ,根据氧化还原反应的配平原则,得失电子守恒,可写出,该反应式为:14HNO3+3Cu2O=6Cu(NO3)2+2NO↑+7H2O;(2)由方程式可知,反应中硝酸生成了Cu(NO3)2和NO,所以体现了硝酸的酸性和氧化性;(3)1mol甲与某浓度硝酸反应时,若还原产物是
,根据氧化还原反应的配平原则,得失电子守恒,可写出,该反应式为:14HNO3+3Cu2O=6Cu(NO3)2+2NO↑+7H2O;(2)由方程式可知,反应中硝酸生成了Cu(NO3)2和NO,所以体现了硝酸的酸性和氧化性;(3)1mol甲与某浓度硝酸反应时,若还原产物是![]() ,则
,则![]() ,若还原产物是
,若还原产物是![]() ,则有
,则有![]() ,在Cu2O一定的情况下,后者消耗的硝酸量更多,所以被还原硝酸的物质的量增加,则产物有
,在Cu2O一定的情况下,后者消耗的硝酸量更多,所以被还原硝酸的物质的量增加,则产物有![]() 生成;
生成;
故答案为:14HNO3+3Cu2O=6Cu(NO3)2+2NO↑+7H2O;酸性;氧化性;使用了较浓的硝酸,产物中有部分二氧化氮生成;
II(4)结合图和已知条件可知,![]() 阶段是反应①,
阶段是反应①,![]() 段是反应②,在
段是反应②,在![]() 段,含碘物质的物质的量没有发生变化,而题上说明只有一种元素的化合价发生变化,所以在
段,含碘物质的物质的量没有发生变化,而题上说明只有一种元素的化合价发生变化,所以在![]() 段是Br的化合价发生变化,此处发生价态归中反应:BrO3-+5Br-+6H+=3Br2+3H2O;(5)根据三段过程可以列出对应的关系式:在
段是Br的化合价发生变化,此处发生价态归中反应:BrO3-+5Br-+6H+=3Br2+3H2O;(5)根据三段过程可以列出对应的关系式:在![]() 阶段有
阶段有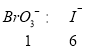 ,
,![]() 段
段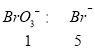 ,
,![]() 段有
段有![]() ,含6 mol KI的硫酸溶液,消耗n(KBrO3)=
,含6 mol KI的硫酸溶液,消耗n(KBrO3)=![]() ;(6)当n(KBrO3)=4时,图像处于
;(6)当n(KBrO3)=4时,图像处于![]() 段,对应反应②2BrO3- +I2 = 2IO3- + Br2,则对应含碘物质的化学式有:I2,KIO3;
段,对应反应②2BrO3- +I2 = 2IO3- + Br2,则对应含碘物质的化学式有:I2,KIO3;
span>故答案为:BrO3-+5Br-+6H+=3Br2+3H2O ;7.2;I2、KIO3。

 阅读快车系列答案
阅读快车系列答案【题目】影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究。
实验一:他们利用Cu、Fe、Mg和不同浓度的硫酸(0.5mol/L、2mol/L、18.4mol/L),设计实验方案来研究影响反应速率的因素。
甲同学研究的实验报告如下表:
实 验 步 骤 | 现 象 | 结 论 |
①分别取等体积的2 mol/L硫酸于试管中; | 反应快慢: | 反应物的性质越活泼, |
(1)该同学的实验目的是_________________________________________;
要得出正确的实验结论,还需控制的实验条件是_____________。
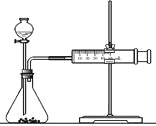
(2)乙同学为了更精确地研究浓度对反应速率的影响,利用下图装置进行定量实验。完成该实验应选用的实验药品可以是(从题中所给药品中挑选)_________________________________________________________;
实验二:
已知: 2KMnO4+5H2C2O4+3H2SO4= K2SO4+2MnSO4+8H2O+10CO2↑,在高锰酸钾酸性溶液和草酸溶液反应时,发现开始一段时间,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快。
(1)针对上述实验现象,某同学认为KMnO4与H2C2O4反应是放热反应,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你的猜想还可能是_______________的影响。
(2)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液试剂外,还需要选择的试剂最合理的是__________________。
A.硫酸钾 B.硫酸锰 C.氯化锰 D.水