题目内容
5.下列实验或生产操作,其中没有新物质生成的是( )①蛋白质溶液中加入硫酸铵后形成沉淀 ②将饱和氯水滴到蓝色石蕊试纸上
③二氧化氮经加压凝成无色液体 ④溴水滴入植物油中振荡褪色
⑤胆矾风化 ⑥除去混在氢氧化铁胶体中的氯化铁.
| A. | ①②③ | B. | ①④⑥ | C. | ③⑤ | D. | ①⑥ |
分析 ①蛋白质溶液中加入无机非重金属盐溶液可发生盐析,使其溶解度降低;
②氯水有强氧化性,能将物质氧化;
③二氧化氮存在2NO2?N2O4 平衡;
④烯烃能使溴水发生加成反应是溴水褪色;
⑤胆矾风化后失水;
⑥溶液中的微粒小于半透膜的孔隙能通过半透膜,而胶体不能通过,所以溶液和胶体的分离方法用渗析.
解答 解:①蛋白质遇到可溶性硫酸铵溶液,会因溶解度降低而从溶液中析出,发生盐析,盐析是可逆的,加水后沉淀又会溶解,是物理变化,无新物质生成,故①正确;
②氯水有强氧化性,能将物质氧化,故有新物质生成,故②错误;
③二氧化氮红棕色,四氧化二氮无色,该反应是一个气体体积减小的可逆反应,加压缩小体积时容器中二氧化氮的浓度增大而使气体颜色加深,继续加压平衡向正方向移动,气体凝成无色液体,由气态变为液态,是化学变化,故③错误;
④植物油中含有碳碳不饱和键,与溴水发生加成反应,使溴水褪色,是化学变化,故④错误;
⑤胆矾风化后失水,由CuSO4•5H2O变为CuSO4,有新物质生成,为化学变化,故⑤错误;
⑥氢氧化铁胶体分散质微粒直径为1nm~100nm不能通过半透膜,氯化铁溶液中的微粒小于半透膜的孔隙能通过半透膜,该法为渗析法分离溶液和胶体,是物理变化,故⑥正确;
故选D.
点评 本题考查物理变化和化学变化,正确理解化学反应的本质有新物质生成是判断化学变化的唯一标准是解答本题的关键,题目难度不大.

练习册系列答案
相关题目
15. A、B、C三种强电解质,它们在水中电离出的离子如表所示:
A、B、C三种强电解质,它们在水中电离出的离子如表所示:
如图1所示装置中,甲、乙、丙三个烧杯依次分别盛放250mL足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极.
接通电源,经过一段时间后,测得乙中c电极质量增加了8g.常温下各烧杯中溶液的pH与电解时间t的关系图如图2.据此回答下列问题:
(1)M为电源的负极(填写“正”或“负”).
(2)计算电极e上生成的气体在标准状况下的体积为2.8L.
(3)B溶液中的溶质为CuSO4.电解后,乙烧杯中溶液的pH=0. 若在B溶液中事先滴加紫色石蕊试液,d极(填写“c”或“d”)先变红.
 A、B、C三种强电解质,它们在水中电离出的离子如表所示:
A、B、C三种强电解质,它们在水中电离出的离子如表所示:| 阳离子 | Na+、K+、Cu2+ |
| 阴离子 | SO${\;}_{4}^{2-}$、OH- |
接通电源,经过一段时间后,测得乙中c电极质量增加了8g.常温下各烧杯中溶液的pH与电解时间t的关系图如图2.据此回答下列问题:
(1)M为电源的负极(填写“正”或“负”).
(2)计算电极e上生成的气体在标准状况下的体积为2.8L.
(3)B溶液中的溶质为CuSO4.电解后,乙烧杯中溶液的pH=0. 若在B溶液中事先滴加紫色石蕊试液,d极(填写“c”或“d”)先变红.
20.下列反应的离子方程式正确的是( )
| A. | NH4HCO3溶液中加入过量NaOH溶液 HCO3-+OH-=H2O+CO32- | |
| B. | 向次氯酸钠溶液中通入少量的CO2 2ClO-+H2O+CO2=2HClO+CO32- | |
| C. | 向乙二酸(H2C2O4)溶液中滴入少量氢氧化钠溶液 H2C2O4+2OH-=C2O42-+2H2O | |
| D. | 氯化亚铁溶液中加入稀硝酸 3Fe2++4H++NO3-=3Fe3++2H2O+NO↑ |
10.事实上,许多非金属氧化物在一定条件下能与Na2O2反应,且反应极有规律,如Na2O2+SO2═Na2SO4
2Na2O2+2SO3═2Na2SO4+O2据此,你认为下列反应方程式中正确的是( )
2Na2O2+2SO3═2Na2SO4+O2据此,你认为下列反应方程式中正确的是( )
| A. | 2Na2O2+2N2O4═4NaNO3 | B. | Na2O2+2NO2═2NaNO2+O2 | ||
| C. | 2Na2O2+2N2O3═4NaNO2+O2 | D. | 2Na2O2+2 Mn2O7═4Na2MnO4+O2 |
15.下列说法正确的是( )
| A. | 298K时,2H2S(g)+SO2(g)═3S(s)+2H2O(l)能自发进行,则其△H>0 | |
| B. | 乙醇、乙二醇、丙三醇互为同系物;H2、D2、T2互为同素异形体 | |
| C. | 用一定浓度的稀盐酸滴定未知浓度的氨水,若选用酚酞作指示剂,会使测定出的氨水物质的量浓度偏低 | |
| D. | 饱和Na2SO4溶液或浓硝酸均可使蛋白质溶液产生沉淀,涉及原理相同 |
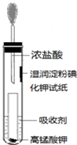 氯气是氯碱工业的主要产品之一,是一种常用的消毒剂,其消毒原理是与水反应生成了次氯酸:Cl2+H2O?HCl+HClO K=4.5×10-4次氯酸的强氧化性能杀死水中的病菌.但是,由于氯气贮运不方便,且具有一定的危险性,目前正逐渐被其他性能优越的消毒产品所替代.请回答:
氯气是氯碱工业的主要产品之一,是一种常用的消毒剂,其消毒原理是与水反应生成了次氯酸:Cl2+H2O?HCl+HClO K=4.5×10-4次氯酸的强氧化性能杀死水中的病菌.但是,由于氯气贮运不方便,且具有一定的危险性,目前正逐渐被其他性能优越的消毒产品所替代.请回答: