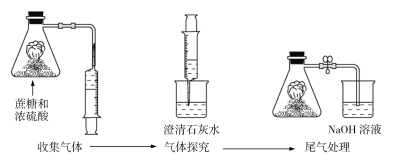
题目内容
【题目】25C时,有关弱酸的电离平衡常数如下表:
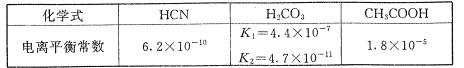
下列有关微粒浓度的说法正确的是( )
A.pH均为8的NaCN溶液、Na2CO3溶液、CH3COONa溶液:c(Na2CO3)>c(NaCN)>c(CH3COONa)
B.浓度均为0.1mol/LNaHCO3和Na2CO3混合溶液中:2c(Na+)=3c(HCO3-)+3c(CO32-)+3c(H2CO3)
C.0.2mol/LHCN溶液与0.lmol/LNaOH溶液等体积混合所得溶液中:c(HCN)>c(Na+)>c(CN-)>c(OH-)
D.浓度均为0lmol/LCH3COOH和CH3COONa混合溶液中:c(CH3COOH)+c(H+)>c(CH3COO-)+c(OH-)
【答案】BC
【解析】
A.酸的电离平衡常数越大,电离程度越大,则酸根离子的水解程度越小,当盐溶液的pH相同时,浓度越大,电离平衡常数:CH3COOH>HCN>HCO3—,则水解程度CO32—>CN—>CH3COO—,所以c(Na2CO3)<c(NaCN)<c(CH3COONa),A选项错误;
B.根据物料守恒可得,浓度均为0.1mol/LNaHCO3和Na2CO3混合溶液中:2c(Na+)=3c(HCO3-)+3c(CO32-)+3c(H2CO3),B选项正确;
C.0.2mol/LHCN溶液与0.lmol/LNaOH溶液等体积混合所得溶液为NaCN和HCN的混合溶液,由于NaCN的水解大于HCN的电离,故有c(HCN)>c(Na+)>c(CN-)>c(OH-),C选项正确;
D。浓度均为0.1mol/LCH3COOH和CH3COONa混合溶液中,醋酸根离子水解程度较小,则c(CH3COOH)+c(H+)<c(CH3COO-)+c(OH-),D选项错误;
答案选BC。

 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案【题目】Ⅰ.甲醇可以与水蒸气反应生成氢气,反应方程式如下:CH3OH(g)+H2O(g)![]() CO2(g)+3H2(g);△H>0
CO2(g)+3H2(g);△H>0
(1)一定条件下,向体积为2L的恒容密闭容器中充入1molCH3OH(g)和3molH2O(g),20s后,测得混合气体的压强是反应前的1.2倍,则用甲醇表示该反应的速率为___。
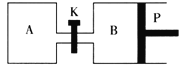
(2)如图中P是可自由平行滑动的活塞,关闭K,在相同温度时,向A容器中充入1molCH3OH(g)和2molH2O(g),向B容器中充入1.2molCH3OH(g)和2.4molH2O(g),两容器分别发生上述反应。已知起始时容器A和B的体积均为aL,反应达到平衡时容器B的体积为1.5aL,维持其他条件不变,若打开K,一段时间后重新达到平衡,容器B的体积为___L(连通管中气体体积忽略不计,且不考虑温度的影响)。
Ⅱ.甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇(于固定容器中进行):2H2(g)+CO(g)![]() CH3OH(g)
CH3OH(g)
下表所列数据是该反应在不同温度下的化学平衡常数(K)
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.27 | 0.012 |
(1)300℃下,将2molCO、6molH2和4molCH3OH充入2L的密闭容器中,判断反应___(填“正向”或“逆向”)进行。
(2)要提高CO的转化率,可以采取的措施是___(填序号)。
a.升温 b.加入催化剂 c.增加CO的浓度 d.加入H2加压 e.加入惰性气体加压 f.分离出甲醇